12, Ene 2022
Ciclo de vida de la información
En la actualidad las instituciones y empresas producen, almacenan y respaldan gran cantidad e información. Hoy en día, la información que posee una empresa es uno de sus valores mas importantes. Este valor no solo es mantener un acceso rápido a los dispositivos que la almacenan. Existen casos donde no se justifica el gasto porque el valor de la información no siempre es el mismo. El veloz crecimiento del volumen de información no puede ser excusa para no organizar esta información según su criticidad y volumen. Cuando la información de una empresa o institución no se encuentra ordenada y clasificada se producen inconvenientes que dificultan su procesamiento ya que se presentan diferentes tiempos de acceso a la información.
El concepto de ciclo de vida esta evolucionado rápidamente en la industria de la información (medianas y grandes empresas) junto al valor que le otorga la información. La idea que sustenta el ciclo de vida es el concepto de la cadena de valor que posee una información en particular desde que se crea hasta que se accede a ella en mayor o menor medida. En estos accesos pasa por una serie de procesos cuya función es añadir valor para quien debe utilizarla hasta agotar su funcionalidad. Sucede que al aumentar el valor de la información también se aumenta el coste de almacenamiento.
Los inconvenientes mencionados surgen ya que el desorden o falta de clasificación se produce por no acceder a la información por los mismos canales o bajo las mismas pautas y los detallamos a continuación.
1.1-Dificultad de acceder a llegar a la información
Mencionábamos que una organización depende de la información que tiene almacenada para poder llevar a cabo sus objetivos. Que el volumen de información esté informatizado no implica que esté de forma ordenada, es decir, que los integrantes de la información sepan cómo, o tengan los medios necesarios para acceder a la información. Éste es el primer obstáculo a superar cuando hablamos de gestionar información dentro del ciclo de vida.
1.2.-Deficiencia en el acceso en cuanto a tiempo y forma
Superado el primer inconveniente, nuestra tarea continua en mejorar el acceso a la información considerando los aspectos técnicos. En esta tarea lo principal es el análisis de los requerimientos de la organización y del relevamiento del hardware disponible para llevar adelante las operaciones.
1.3.-Diferentes modos de acceder a la información
Por último, pondremos foco en mejorar el acceso a la información teniendo presente los aspectos externos al hardware y dependientes de cada uno de los usuarios o áreas que necesitan acceder.
Muchas veces para mitigar o corregir parcialmente estos inconvenientes se intenta alojar la mayor cantidad de información en servidores con discos duros (de alto rendimiento). Ya que el alojamiento en estos servidores ayudan a mantener, gestionar, hacer peticiones y establecer conexiones de bases de datos que ayudan con el orden de información.
Ya hemos dicho que el significado y la importancia de esta información serán los mismos a medida que transcurre el tiempo. Debido a esto la forma, los métodos y las técnicas con que debe ser almacenada y respaldada la información cambiaran de acuerdo al paso del tiempo, ya que la información no tendrá el mismo valor, es decir, el concepto principal que obtenemos del ciclo de vida de la información es almacenar la información donde podremos obtener el mejor beneficio de ella.
Relevar y analizar los puntos antes mencionados nos proporcionaran una idea muy acertada de cómo encarar al almacenamiento y, si fuera necesario, protección (backups) de la información concerniente al sistema que estamos analizando, diseñado o administrando.
No olvides que en caso de ser necesario, puedes contactarnos para mejorar el proceso de laboratorio y administrativo de tu organización a través software 100% confiable y seguro. Recuerda que en deappharma somos expertos en la materia, por lo que procesos complejos no representa un reto para nosotros, debido a que tenemos en mente los aspectos relevantes de cumplimiento.
Referencia;
- Administración de Storage y Backups_Dante cantone, España, Editorial Alfa Omega
¡Contáctanos! y conoce de que manera te vamos a ayudar.
¡Únete a nuestra comunidad en redes!
- 0
- Por Team deappharma
29, Jun 2021
Revisión de estado validado de método analíticos.
Uno de los varios procesos de control analítico dentro de la industria, es el seguimiento o mantenimiento del estado validado y/o estado de control de métodos analíticos. No es una tarea fácil!! ya que para realizar una correcta revisión, el entorno en el que gira el proceso de mantenimiento validado radica en el acceso a documentos y en la obtención de datos que se asocian directamente a la esencia del método, como son: primera validación y parámetros de adecuabilidad históricos.
Concepto:
El concepto de ciclo de vida, vincula el desarrollo de productos y procesos, por lo que se debe adquirir conocimiento para abordar la revisión.
Validación métodos y calidad de los medicamentos.
La validación efectiva del método contribuye significativamente a asegurar la calidad de los medicamentos. Lo básico, es comprender el principio de garantía de calidad. Este principio describe que se debe producir un medicamento que sea apto para el uso previsto.
Este principio incorpora el entendimiento de que existen las siguientes condiciones:
a) La calidad, la seguridad y la eficacia están diseñadas o integradas en el producto.
b) La calidad no puede garantizarse adecuadamente simplemente mediante el producto en proceso y terminado, inspección o prueba.
Un programa de validación exitoso depende de la información y el conocimiento del método, así como, de la comprensión del proceso de desarrollo analítico. Este conocimiento es la base para establecer un enfoque para el control del analítico, que da como resultado certidumbre en la calidad y atributos evaluados. Los científicos analíticos deben:
- Comprender las fuentes de variación (se puede evaluar durante la validación o con la revisión de los datos de validación).
- Detectar la presencia y el grado de variación (análisis de datos obtenidos en la validación y en el histórico de datos de liberación, sin embargo, esto no mide directamente el método).
- Controlar la variación de una manera acorde con el riesgo, que representa para el método que afecta los datos de liberación del producto.
Descripción del proceso analítico en tres etapas:
Etapa 1 – Diseño del proceso analítico: el proceso analítico se define durante este etapa, basada en el conocimiento adquirido a través de actividades de desarrollo.
Etapa 2 – Validación del proceso analítico: durante esta etapa, el diseño analítico se evalúa para determinar si método es capaz de producir resultados reproducibles.
Etapa 3 – Verificación continua del proceso analítico: la garantía continua se obtiene durante la rutina analítica, de tal manera, que se pueda verificar que el proceso permanece en un estado de control.
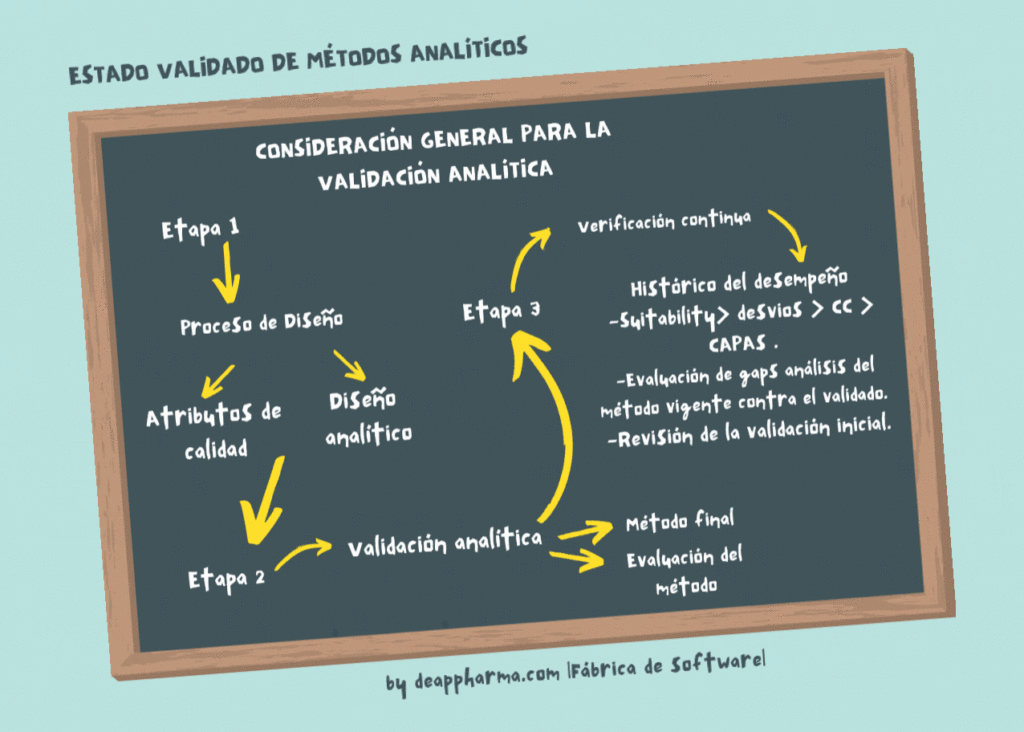
Los puntos relevantes de evaluación a la etapa 3, son:
- Requisitos de idoneidad históricos del sistema (platos teóricos, resolución, factor de coleo, factor de simetría, factor de capacidad y/o tiempos de retención de componentes).
- Parametrización y evaluación de las pruebas de desempeño acordes al método analítico.
- Revisión de los ajustes a las condiciones de operación indicadas en el procedimiento analítico vigente vs los descritos en la validación y/o transferencia inicial.
- Hallazgos o desviaciones, directamente relacionadas al desempeño del método analítico.
Si una evaluación basada en riesgos es utilizada como herramienta, se deben considerar otros factores. Los cuales pueden conducir a cambios en un procedimiento analítico y/o reemplazo con un nuevo método, se puede considerar los siguiente:
- Un ejercicio nuevo de transferencia;
- Una posible revalidación, sea parcial o total, o,un nuevo ejercicio de validación o,
- Un estudio de comparabilidad de métodos analíticos, es una opción factible.
En algunos casos, cambios en el fármaco o sustancias dentro del proceso de fabricación también deben ser evaluados como parte de la revisión de estado validado.
Recurso analítico «software».
Como se menciono anteriormente, la revisión de estado validado de un método analítico radica en que tan disponible y correcta fue la ejecución de este. Por lo que, la disposición de la información debe ser consistente. De otra manera será difícil concluir.
eADMxL el software de cumplimiento de deappharma.com , le ayudara con el control del proceso de estado validado mediante sus funciones especificas de «Revisión de estado validado» y «Monitoreo de vigencias».
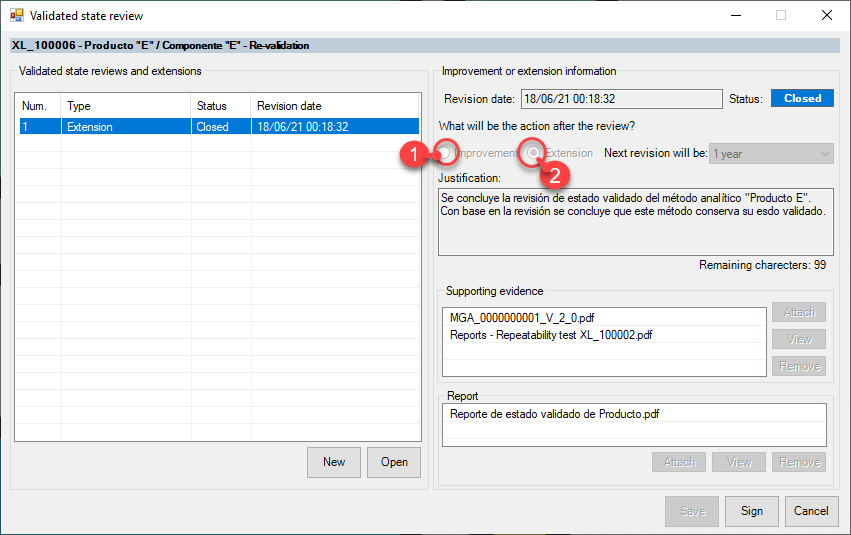
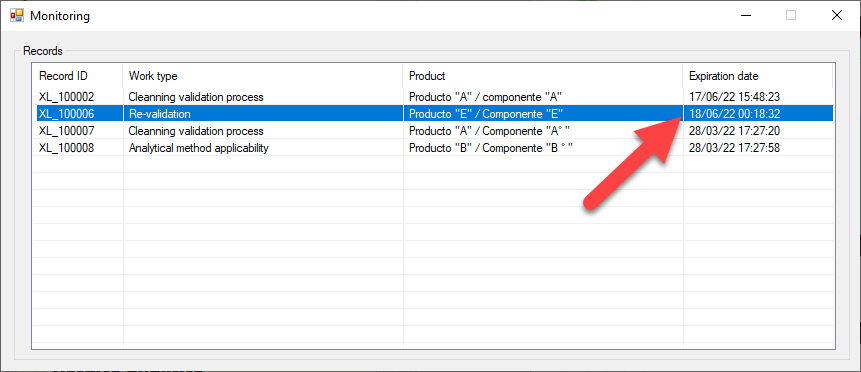
Algunas preguntas relevantes, que le ayudaran a definir el estado de control y/o mantenimiento, son:
- El método fue planteado y validado en concordancia con su categoría?
- La estadística paramétrica es integra?
- Los resultados de validación analítica son consistentes y claros?
- Si es un método compendial, los datos de pruebas de robustez tolerados están documentados?
- Los criterios de “Suitability” del sistema, se mantienen a través de los análisis?
- Las condiciones analíticas establecidas en el método final (preparación , condiciones de análisis, columna etc.) son las mismas que están descritas en el reporte de validación del método?
- Si hay cambios al método, se registran y se alinean a un control de cambio y se emite un CaPa al método y con esto evaluar el impacto a la validación?
- Qué tan recurrentes son las desviaciones o justificaciones asociadas al método analítico?
- Si la validación analítica sigue vigente, puedo hacer un revisión de estado validado antes de su fin expiración si surgen problemas?
No olvides que en caso de ser necesario, puedes contactarnos para mejorar el proceso de laboratorio y administrativo de tu organización a través software 100% confiable y seguro. Recuerda que en deappharma somos expertos en la materia, por lo que procesos complejos no representa un reto para nosotros, debido a que tenemos en mente los aspectos relevantes de cumplimiento.
Referencias.
- Analytical Procedures and Methods Validation for Drugs and Biologics Guidance for Industry
- Pharmaceutical quality system ICH Q10.
- Guidance for Industry Process Validation: General Principles and Practices.
¡Contáctanos! y conoce de que manera te vamos a ayudar.
¡Únete a nuestra comunidad en redes!