4, Feb 2025
Beneficios de un software de gestión documental
Optimización y eficiencia en la era digital

Un software de gestión documental ofrece una amplia gama de beneficios para las organizaciones, facilitando la administración y el control de documentos de manera eficiente y segura. A continuación, se detallan algunos de los principales beneficios:
Acceso rápido y eficiente a la información
Un sistema de gestión documental permite almacenar, organizar y recuperar documentos de manera rápida y sencilla. Gracias a sus capacidades de búsqueda avanzada, los usuarios pueden encontrar la información que necesitan en cuestión de segundos, mejorando la productividad y reduciendo el tiempo dedicado a la búsqueda de documentos.
Reducción de costos
La digitalización de documentos y el uso de un software de gestión documental reduce significativamente los costos asociados con el almacenamiento físico, la impresión y la distribución de documentos en papel. Además, disminuye la necesidad de espacio físico para archivar documentos, lo que puede generar ahorros adicionales en alquileres y mantenimiento.
Mejora en la colaboración
Un sistema de gestión documental permite a los equipos trabajar de manera colaborativa en documentos, independientemente de su ubicación geográfica. Los usuarios pueden acceder, editar y compartir documentos en tiempo real, lo que facilita la colaboración y la toma de decisiones en equipo.
Mayor seguridad y control
Los sistemas de gestión documental ofrecen múltiples capas de seguridad para proteger la información sensible. Esto incluye controles de acceso, cifrado de datos y registros de auditoría que permiten rastrear quién accede, edita o elimina documentos. De esta manera, se garantiza la confidencialidad y la integridad de la información.
Cumplimiento normativo
La mayoría de los sistemas de gestión documental están diseñados para cumplir con regulaciones y estándares específicos de la industria. Esto facilita a las organizaciones adherirse a normativas legales y de seguridad, evitando sanciones y garantizando la correcta gestión de la documentación.
Automatización de procesos
Un software de gestión documental permite automatizar tareas repetitivas y procesos administrativos, como la captura, clasificación y almacenamiento de documentos. Esto no solo reduce el riesgo de errores humanos, sino que también libera tiempo para que los empleados se enfoquen en actividades de mayor valor añadido.
Sostenibilidad ambiental
La reducción del uso de papel contribuye a la sostenibilidad ambiental, disminuyendo la huella de carbono de las organizaciones. La digitalización y el uso de un software de gestión documental promueven prácticas más ecológicas y responsables con el medio ambiente.
Escalabilidad y adaptabilidad
Los sistemas de gestión documental son escalables y pueden adaptarse a las necesidades cambiantes de las organizaciones. A medida que una empresa crece, el software puede ajustarse para manejar un mayor volumen de documentos y usuarios, garantizando un rendimiento óptimo en todo momento.
En resumen, un software de gestión documental ofrece numerosos beneficios que mejoran la eficiencia, reducen costos, aumentan la seguridad y fomentan la colaboración. Es una herramienta esencial para cualquier organización que desee optimizar sus procesos y mantenerse competitiva en la era digital.
Te invitamos a conocer una solución confiable que te ayudara a brindar atributos ALCOA++ a tus hojas de cálculo y documentos. En Deappharma hemos desarrollado, eDocuSeed un software que centraliza todos tus libros de Excel y documentos en un solo puntos brindándoles los atributos de integridad de datos necesarios para dar cumplimiento a las regulaciones más exigentes. Nuestra solución ya impacta de manera positiva a empresas del sector farmacéutico, dispositivos médicos y distribuidoras de medicamentos. Solicita tu demostración totalmente gratuita. ¡Estamos listos para ayudarte!
Contáctanos en https://deappharma.com/contacto/ y solicita una demostración y asesoría gratuita.
¡Gracias por leernos!
- 0
- Por Team deappharma
12, Abr 2023
Definiendo los requerimientos de usuario
Una clave muy importante para la validación del software y libros de Excel es una especificación documentada de los requisitos que defina:
– el «uso previsto» del software, libro de Excel o equipo automatizado; y
– la medida en que el fabricante del producto depende de ese software, libro de Excel o equipo para la producción de un producto sanitario de calidad.
El fabricante del producto (usuario) tiene que definir el entorno operativo previsto, incluyendo cualquier configuración de hardware y software necesarias, versiones de software, utilidades, etc. El usuario también debe:
– documentar los requisitos de rendimiento del sistema, calidad, gestión de errores, puesta en marcha, apagado, seguridad, etc;
– identificar cualquier función o característica relacionada con la seguridad, como sensores, alarmas, enclavamientos, pasos lógicos de procesamiento o secuencias de comandos; y
– definir criterios objetivos para determinar el rendimiento aceptable.
La validación debe realizarse de acuerdo con un protocolo documentado, y los resultados de la validación también deben documentarse. Deben documentarse los casos de prueba que pongan a prueba el rendimiento del sistema con respecto a los criterios predeterminados, especialmente para sus parámetros más críticos.
Los casos de prueba deben abordar las condiciones de error y alarma, el arranque, el apagado, todas las funciones de usuario y controles de operador aplicables, posibles errores de operador de valores permitidos y las condiciones de estrés aplicables al uso previsto del equipo. Los casos de prueba deben ejecutarse y los resultados deben registrarse y evaluarse para determinar si los resultados permiten concluir que el programa informático está validado para el uso previsto.
Un fabricante de productos puede llevar a cabo una validación utilizando su propio personal o puede depender de un tercero, como el fabricante del equipo/software tercero, o un consultor. En cualquier caso, el fabricante del producto conserva la responsabilidad última de garantizar que el software del sistema de producción y calidad:
– se valide de acuerdo con un procedimiento escrito para el uso concreto previsto; y
– funcionará según lo previsto en la aplicación elegida.
El fabricante del producto debe disponer de documentación que incluya
– los requisitos de usuario definidos
– el protocolo de validación utilizado
– los criterios de aceptación
– casos de prueba y resultados; y
– un resumen de validación que confirme objetivamente que el software y/o Libros de Excel está validado para el uso previsto.
¿Existen herramientas en el mercado que mejoren los procesos administrativos y de laboratorio?
Como bien sabemos el desafío más grande al que se a puesto a prueba el sector farmacéutico es el relacionado con la integridad de datos. ¡Pero! ¿Por qué es tan complejo este tema? La respuesta se deriva por la gran cantidad de datos y documentos que se emiten día con día en el que se ven impactados documentos y libros de Excel.
Recordemos que la validación de software y libros de Excel es el primer paso. No obstante, muchos libros de Excel utilizados en el sector farmacéutico no cuentan con evidencia de validación lo cual es un riesgo que podrá derivar en un hallazgo critico ante una inspección regulatoria.
El segundo paso y el más complejo es adherir las configuraciones necesarias que eleven la integridad de datos y favorezcan el mantenimiento tanto de software como de Libros de Excel.
Te invitamos a mitigar el riesgo por el uso de sistemas computarizados no validados y con pobres atributos de integridad de datos. Nuestros desarrollos están estructurados bajo un sistema de gestión de calidad trazable y auditable. Tales cuales cuentan con el soporte de validación-calificación documental con base en Gamp 5 y CFR21 parte 11.
Conoce eADMxL el cual es un software que desarrollamos para mitigar el uso de hojas de cálculo para procesos de validación de métodos analíticos. Conoce sus beneficios y alcance general aquí: ¡Da clic aquí!
eDocuSeed es más que un software de gestión documental ya que este es capaz de controlar y mantener libros de Excel por medio de adición de controles necesarios para: acceso, edición, trazabilidad y su mantenimiento. Conoce sus beneficios y alcance general aquí: ¡Da clic aquí!
“No vivas con el riesgo ¡Mitígalo!” para eso nosotros de ayudamos.
Visita nuestro sitio www.deappharma.com y solicita una demostración y asesoría gratuita.
¡Contáctanos! y conoce de que manera te vamos a ayudar.
¡Únete a nuestra comunidad en redes!
20, May 2022
Linealidad del sistema
Es la capacidad del método analítico para obtener resultados directamente proporcionales a la concentración o cantidad del analito en un rango definido.
La linealidad puede demostrarse directamente en la sustancia farmacológica (mediante dilución de una solución madre estándar) y/o pesadas separadas de mezclas sintéticas de los componentes del producto farmacéutico, utilizando el procedimiento propuesto. Este último aspecto puede estudiarse durante la investigación en el rango definido. La linealidad debe evaluarse mediante la inspección visual de un gráfico de señales en función de la concentración o el contenido del analito. Si existe una relación lineal, los resultados del ensayo deben evaluarse mediante métodos estadísticos apropiados, por ejemplo, mediante el cálculo de una línea de regresión por el método de los mínimos cuadrados. En algunos casos, para obtener la linealidad entre los ensayos y las concentraciones de la muestra, puede ser necesario someter los datos del ensayo a una transformación matemática antes del análisis de regresión. Los datos de la línea de regresión pueden ser útiles para proporcionar estimaciones matemáticas del grado de linealidad.
Deben presentarse valores tales como:
Coeficiente de correlación (r). Muchos autores planteanque para que el método se considere lineal, el coeficiente de correlación debe ser mayor que 0,999. Sin embargo, la mejor forma de indicar la linealidad del método estudiado será realizar una prueba estadística de t (t de Student), en la cual se calculará la correlación lineal significativa (tr) a partir de la hipótesis nula de no correlación entre las magnitudes estudiadas («x» y «y«).
Pendiente (conocida también como coeficiente de regresión). Indica la sensibilidad de calibración o del método y se expresa en unidades de respuesta sobre unidades de concentración o cantidad del analito. La sensibilidad analítica relaciona la aleatoriedad de la respuesta con la aleatoriedad debida a la variación de la concentración, es inversamente proporcional a la capacidad de detectar pequeñas diferencias en la concentración del analito, y se obtiene dividiendo la pendiente de la curva de calibración por la desviación estándar de las respuestas en cada punto o concentración. Se considera que, a mayor pendiente, mayor sensibilidad y que mientras más pequeño sea el coeficiente de variación de la pendiente mayor será la linealidad (coeficientes de variación de la pendiente mayores que el 5,0 % indican falta de linealidad).
Intercepto. Es el estimador que se relaciona con la presencia de interferencias o errores sistemáticos. El intervalo de confianza del intercepto debe incluir al cero para cumplir con el requisito de proporcionalidad (como se exige para el cumplimiento de la ley de Lambert-Beer en los métodos espectrofotométricos). Se determinará la prueba de proporcionalidad mediante una prueba t considerando como hipótesis nula que el intercepto tiene que ser cero.
La intersección y la pendiente de la línea de regresión, así como la suma residual de los cuadrados. Debe incluirse un gráfico de los datos (reporte). Además, deberá presentarse un análisis de la desviación de los puntos de datos reales con respecto a la línea de regresión puede ser útil para evaluar la linealidad.
Algunos procedimientos analíticos, como los inmunoensayos, no demuestran linealidad
después de cualquier transformación. En este caso, la respuesta analítica debe describirse mediante una función apropiada de la concentración (cantidad) de un analito en una muestra. Para establecer la linealidad, se recomienda un mínimo de 5 concentraciones. Deberán justificarse otros enfoques.
Proceso de linealidad del sistema controlado y gestionado con eADMxL.
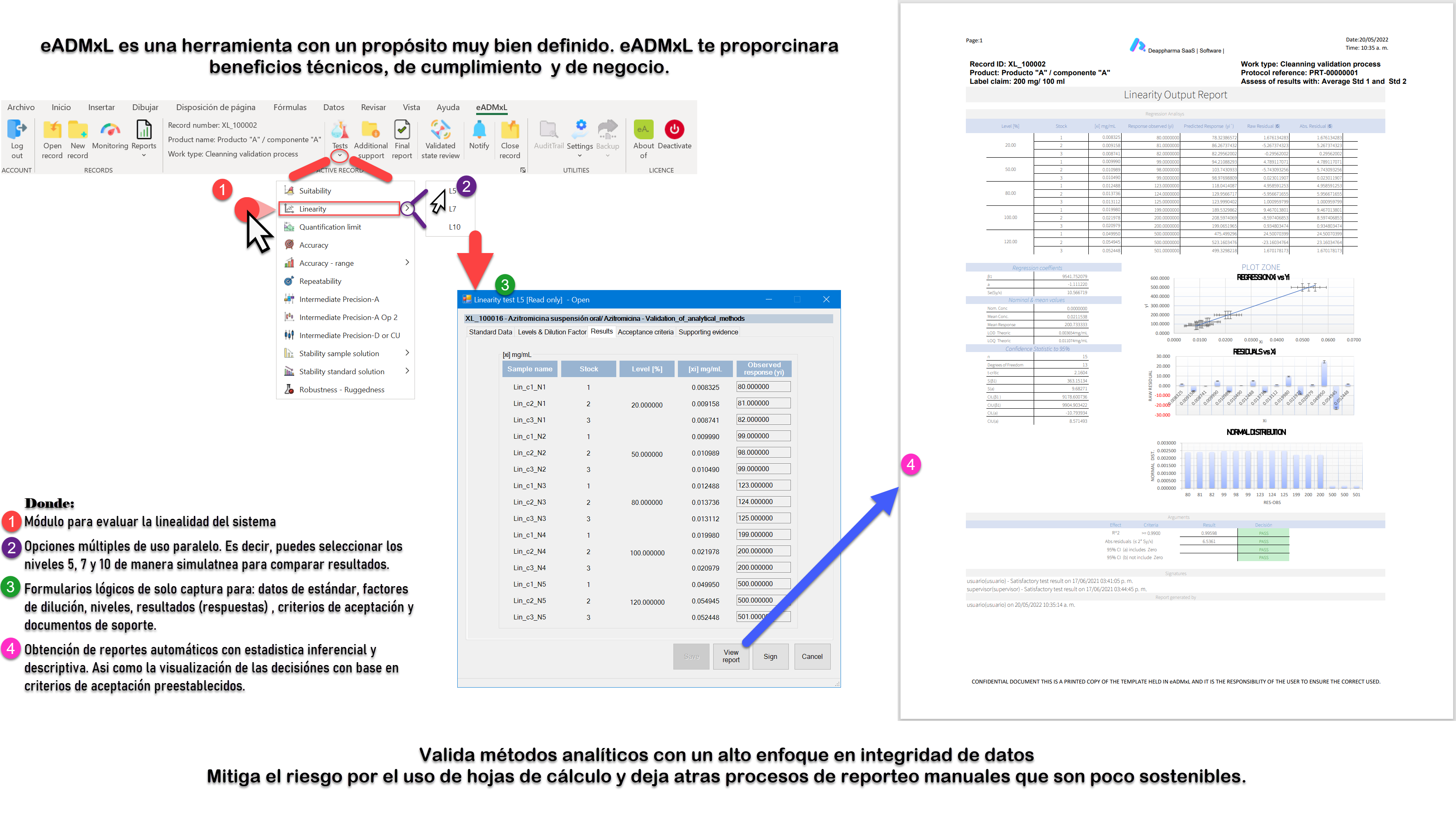 No olvides que, en caso de ser necesario, puedes contactarnos para mejorar el proceso de laboratorio y administrativo de tu organización a través software 100% confiable y seguro. Recuerda que en deappharma contamos con un software que te ayudara a controlar tu proceso de validación de métodos analíticos. Somos expertos en la materia, por lo que procesos complejos no representa un reto para nosotros, debido a que tenemos en mente los aspectos relevantes de cumplimiento.
No olvides que, en caso de ser necesario, puedes contactarnos para mejorar el proceso de laboratorio y administrativo de tu organización a través software 100% confiable y seguro. Recuerda que en deappharma contamos con un software que te ayudara a controlar tu proceso de validación de métodos analíticos. Somos expertos en la materia, por lo que procesos complejos no representa un reto para nosotros, debido a que tenemos en mente los aspectos relevantes de cumplimiento.
Referencias
- Rampazoo P. Standardisation and validation of analytical methods in the pharmaceutical industry. Il Farmaco 1990; 45:807-15.
- Comellas L. Desarrollo de métodos en HPLC. Barcelona: Instituto Químico de Sarria, 1994:68.
- VALIDATION OF ANALYTICAL PROCEDURES: TEXT AND METHODOLOGY Q2(R1)
¡Contáctanos! y conoce de que manera te vamos a ayudar.
¡Únete a nuestra comunidad en redes!