31, Oct 2023
Validación de hojas de cálculo (Instalación, seguridad y buenas prácticas)
En industria regulada es de vital importancia el cumplimiento a lo descrito en las normas aplicables: NOM-059, NOM-241 etc. Recordemos que el cumplimiento a los requerimientos establecidos en estos documentos es de carácter obligatorio. Es una realidad que el hacer cumplir los requerimientos en muchos casos se torna una tarea compleja por la dimensión de interpretación que le puedas dar a cada requerimiento regulatorio establecido. Sin embargo, es importante mencionar que existen una serie de documentos, guías y referencias de otras entidades regulatorias que dan apoyo y complementan de manera correcta la interpretación para aquellos requerimientos en los cuales no sea claro el entregable.
Cuando hablamos de validación de sistemas computarizados debemos tener presente que los puntos normativos no solo se refieren a validar: ERP, SAP, softwares comerciales, softwares personalizados o softwares estructurados y diseñados a las medidas, por mencionar algunos. Recordemos que una hoja de Excel normativamente se considera un sistema computarizado. Tales cuales, en muchas ocasiones estos archivos son categorizados con en nivel máximo de complejidad y criticidad que impactan los procesos de las buenas prácticas BxP (GxP).
Esta serie de artículos tendrá como finalidad explicarte el enfoque de validación de hojas de cálculo establecido en el Anexo 1 de la Directriz Europea.
Durante nuestra experiencia hemos conocido diferentes magnitudes de riesgos asociados al control, gestión y mantenimiento de hojas de cálculo. Hemos conocido empresas que no cuentan con área de validación o empresas que por la rutina diaria no disponen del tiempo para ejecutar la acción. De cualquier manera, esto no los deja exentos de cumplir la normatividad.
Todos sabemos que Excel es una herramienta altamente versátil y dinámica utilizada diariamente. Sin embargo, esta versatilidad le impregna un alto riesgo por el grado de personalización que estas pueden llegar a tener en su diseño y función y que impactan en la toma de decisiones.
El Anexo 1 de la Directriz Europea para la validación de hojas de cálculo «Validación de sistemas informatizados», debe utilizarse a la hora de planificar, realizar y documentar la validación.
Este anexo presenta un ejemplo de validación de hojas de cálculo Excel, que debe utilizarse en combinación con los requisitos y recomendaciones generales que figuran en el documento referente y/o lo establecido en la regulación local aplicable.
INSTALACIÓN Y SEGURIDAD
Para garantizar que sólo se utiliza la última versión validada de la hoja de cálculo y mantener el estado validado de la hoja de cálculo, todas las hojas de cálculo Excel validadas deben almacenarse con derechos de acceso de sólo lectura para los usuarios finales (por ejemplo, en un recurso compartido de red protegido o algo con mucha mayor robustez en seguridad un software de control y mantenimiento como lo es DocuSeed). Sólo las personas responsables deben tener acceso de escritura a la red compartida.
Los usuarios finales no deben tener derecho a modificar una hoja de cálculo validada, añadir una hoja de cálculo no validada al recurso compartido ni guardar datos en él. Los usuarios finales sólo deben tener derecho a rellenar las celdas (permitidas) e imprimir los datos o guardar una copia en un repositorio de datos en caso necesario.
La instalación deberá documentarse, por ejemplo, en el archivo de validación, en un libro de registro del sistema o en un formulario de control de calidad. Se documentará el nombre de la hoja de cálculo, la identificación única, la localización y la persona responsable de la hoja de cálculo según aplique. Los registros también incluirán la verificación, la verificación periódica y otras cuestiones como las actualizaciones o cualquier problema encontrado. La verificación se completará tras instalación y se registrará.
BUENAS PRÁCTICAS
Al configurar una nueva hoja de cálculo, seguir las siguientes buenas prácticas reducirá el riesgo de modificaciones accidentales de la plantilla e introducción de datos erróneos:
– Todas las celdas de cálculo deberán estar bloqueadas (Formato de celdas > Protección > Bloqueadas) para proteger las celdas que contengan cálculos contra modificaciones involuntarias, excepto las utilizadas para la introducción de datos.
-Las celdas utilizadas para la introducción de datos pueden identificarse mediante un color específico.
– Las reglas de validación de datos (pestaña Datos > Validación de datos) pueden aplicarse a las celdas de entrada de datos para evitar la introducción de valores aberrantes (siempre y cuando exista un requerimiento de especificación previamente establecido). Los mensajes de entrada y los mensajes de alerta de error para informar al usuario final del tipo de datos esperado y del rango aceptable.
Las celdas utilizadas para presentar los resultados de los cálculos (salida) pueden identificarse mediante un color específico. Cuando los resultados se comprueban en función de criterios de aceptación, se recomienda utilizar el formato condicional (pestaña Inicio > Formato condicional) para resaltar los resultados fuera de especificación.
-El nombre del operador responsable de la introducción de los datos, así como la fecha y la hora de introducción de los datos deben registrarse en las celdas de entrada específicas o la hoja de cálculo se imprime, firma y fecha después del cálculo.
– La ruta del archivo, el nombre del archivo de la hoja de cálculo y el número de versión de MS Excel® pueden mostrarse en el área de impresión de la hoja de cálculo. Las funciones de Excel ‘=CELL(«filename»)’ ‘=INFO(«RELEASE»)’ pueden utilizarse para mostrar la ruta, el nombre de archivo, la hoja activa y el número de versión de MS Excel® en uso.
-Se recomienda proteger con contraseña todas las celdas que contengan cálculos (pestaña Revisar >Proteger hoja), con sólo las opciones por defecto marcadas. Se puede utilizar la misma contraseña para todas hojas y puede documentarse en el archivo de validación. La contraseña de protección de la hoja no debe comunicarse a los usuarios finales.
-Después de proteger cada hoja, la estructura del libro de trabajo también debe protegerse con contraseña (pestaña Revisar > Proteger libro). Se puede utilizar la misma contraseña que para la protección de las hojas.
Como lo podemos percibir la etapa de validación de hojas de cálculo esencialmente refiere a la estructuración documental del diseño y funcionamiento para el propósito requerido. En esta etapa no se establece como alcance regulatorio el mantenimiento de estos archivos con propiedades ALCOA++. El tema de fases de validación y mantenimiento de estos archivos los abordaremos en otro artículo.
Te invitamos a conocer una solución confiable que te ayudara a brindar atributos ALCOA++ a tus hojas de cálculo validadas. En deappharma hemos desarrollado, eDocuSeed un software que centraliza todos tus libros de Excel en un solo puntos brindándoles los atributos de integridad de datos necesarios para dar cumplimiento a las regulaciones más exigentes. Nuestra solución ya impacta de manera positiva a empresas del sector farmacéutico, dispositivos médicos y distribuidoras de medicamentos. Solicita tu demostración totalmente gratuita. ¡Estamos listos para ayudarte!
Contáctanos en https://deappharma.com/contacto/ y solicita una demostración y asesoría gratuita.
¡Gracias por leernos!
- 0
- Por Team deappharma
3, Jul 2023
Hojas de cálculo; categorización conforme a GAMP 5
Las hojas de cálculo pueden ser tan complejas o simples según la necesidad de la actividad a realizar. Sin embargo, al momento de evaluar una hoja de cálculo el proceso es mucho más sistemático de lo que se cree. Te invitamos a leer nuestro siguiente articulo y conoce algunos detalles relevantes que te ayudaran a categorizar tu hoja de cálculo.
Enfoque basado en el riesgo
Una aplicación de hoja de cálculo puede variar significativamente en cuanto a riesgo y complejidad. No obstante, en todos los casos es necesario cumplir los siguientes requisitos:
- Evaluación del riesgo y medidas de control del riesgo apropiadas para gestionar el riesgo identificado.
- Especificación y verificación apropiadas para demostrar que la aplicación funciona según lo previsto.
La estrategia de especificación y verificación de la aplicación que se está construyendo debe basarse en:
- El impacto del sistema en la seguridad del paciente, la calidad del producto y la integridad de datos mediante la evaluación del riesgo.
- Complejidad y novedad del sistema (arquitectura y categorización de los componentes del sistema).
- La seguridad apropiada para mitigar el riesgo de cambios no autorizados en los datos o la aplicación.
Es importante mencionar que el proceso de validación de sistemas computarizados en los cuales están incluidas las hojas de cálculo deben estar regidas por políticas y procedimientos de la empresa para definir y lograr mantener la conformidad y la idoneidad para el uso previsto de la aplicación por el usuario final.
Uso de categorías GAMP 5
La categorización de hojas de cálculo se debe establecer con base en la guía GAMP 5. La guía nos proporciona lineamiento y algunos ejemplos generales que nos ayudan a comprender el rumbo a tomar para realizar el proceso de validación de este tipo de archivos.
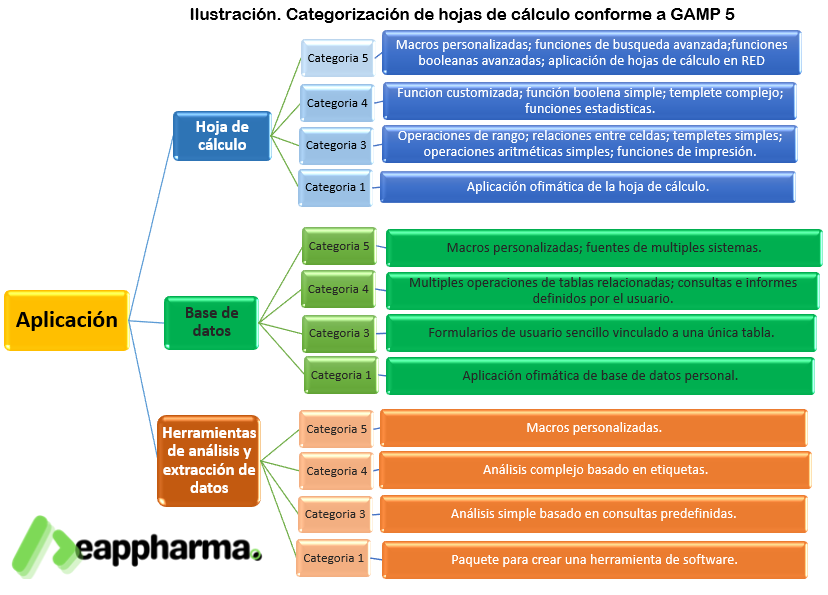
GAMP 5 establece y define 4 categorías de clasificación siendo las siguientes; 1, 3, 4 y 5. A continuación se describen criterios y detalles con base en esta Guía.
La herramienta sobre la que se construye la aplicación, como el paquete de hoja de cálculo, debe considerarse como categoría 1.
Las categorías para hojas de cálculo y otras aplicaciones de usuario final deben considerarse como un continuo que abarca las categorías 3, 4 y 5. La asignación de una categoría depende de la complejidad y personalización de la hoja de cálculo o aplicación. No obstante, hay que tener en cuenta que una hoja de cálculo que se limita a utilizar la capacidad de esta para edición, tabulación y no realiza ningún cálculo debe considerarse un documento. El uso previsto de los datos ensayados debe tenerse en cuenta a la hora de determinar los requisitos de verificación y el control que debe establecerse. Una simple hoja de cálculo (categoría 3) puede presentar un riesgo BxP (o GxP) elevado en función del uso que se haga de los datos.
Una hoja de cálculo que simplemente utiliza funciones nativas para realizar cálculos en lugar de una calculadora de mano suele ser de categoría 3. Por ejemplo, un analista de laboratorio puede crear una hoja de cálculo única para realizar un cálculo relacionado con una investigación derivado de un fuera de especificación. Cuando se utiliza la función aritmética de las hojas de cálculo, el cálculo debe explicarse detalladamente. Los datos deben explicarse de la misma manera que en un documento de texto. Esto debe incluir la verificación de que el cálculo se ha realizado correctamente y que los datos analizados son los correctos. Esta verificación podría documentarse fácilmente haciendo que otro analista o un supervisor examinara la hoja de cálculo y la aprobara. No se requiere ninguna otra verificación, ya que no es necesario cuestionar la exactitud del cálculo.
Cuando se desarrollen hojas de cálculo como templetes, podrían ser de categoría 3 a 5, dependiendo de la complejidad. Para el propósito de la aplicación de usuario, la definición de la categoría 4 se altera ya que esta se centra en la complejidad frente a la configurabilidad.
Por ejemplo:
- Un analista utiliza un templete en el laboratorio para realizar un cálculo rutinario de medias y desviación estándar de resultados experimentales. Se trata de una operación aritmética directa sin configuración, por lo que el templete es de categoría 3.
- Un templete de hoja de cálculo requiere que el usuario introduzca la dureza de la tableta, por lo que la aplicación se ramifica automáticamente a diferentes celdas (customs) para utilizar el cálculo específico de la dureza basado en esta entrada. Una operación tan simple haría que la hoja fuera de categoría 4, ya que tiene alguna operación booleana (es decir, celdas vinculantes o condicionales lógicas a otras celdas para procesar datos de entrada) simple basada en la entrada del usuario.
- Una aplicación de hoja de cálculo que emplee macros personalizadas o una lógica anidada sofisticada para obtener resultados o una función de búsqueda debería tratarse como categoría 5.
En la siguiente ilustración podrás observar el alcance generar por aplicación y la relación que estas tienen respecto a sus diferentes categorías.
¿Existen herramientas en el mercado que mejoren los procesos de control y mantenimiento de libros de Excel?
Como bien sabemos el desafío más grande al que se ha puesto a prueba el sector farmacéutico es el relacionado con la integridad de datos. Derivado de la gran cantidad de datos emitidos día con día en el que se ven impactados documentos y libros de Excel.
Recordemos que la validación de hojas de cálculo es el primer paso. No obstante, muchos libros de Excel que contienen hojas de cálculo utilizados en el sector farmacéutico no cuentan con evidencia de validación lo cual es un riesgo que podrá derivar en un hallazgo critico ante una inspección regulatoria. El segundo paso y el más complejo es adherir las configuraciones necesarias que eleven la integridad de datos y favorezcan la gestión y el mantenimiento de estas con base en GAMP 5 y CFR21.
En la actualidad el trabajo realizado y el menos sugerible es la configuración de control de seguridad y trazabilidad sobre usos de hojas de cálculo con el uso de VBA lo cual es meramente simbólico que a mediano y largo plazo será poco sostenible en términos de cumplimiento e integridad de datos.
En deappharma tenemos la solución para mitigar tu riesgo por el uso de hojas de cálculo no validadas y con deficiencias en los atributos de control de integridad de datos. Hemos logrado automatizar el proceso y, con esto ahorres tiempo, dinero y esfuerzo para dar el cumplimiento regulatorio requerido. Nuestros desarrollos están estructurados bajo un sistema de gestión de calidad trazable y auditable y, tales cuales cuentan con el soporte de validación-calificación que garantizan la precisión del alcance del diseño establecido.
Estamos convencidos de que eDocuSeed te ayudara a mitigar el uso de hojas de cálculo y dar ese paso de cumplimiento que necesitas. Conoce sus beneficios y alcance general aquí: ¡Da clic aquí!
“No vivas con el riesgo ¡Mitígalo!” para eso nosotros de ayudamos.
Visita nuestro sitio www.deappharma.com y solicita una demostración y asesoría gratuita.
¡Contáctanos y únete a nuestra comunidad en redes!
21, Abr 2023
Validación/Verificación de procedimientos analíticos enfoque EDQM
La directriz de la ICH sobre «Validación de procedimientos analíticos: Texto y Metodología» (Q2) constituye un análisis de las características de validación que deben tenerse en cuenta durante la validación de un procedimiento analítico (la directriz también se ha adoptado para los veterinarios durante el debate de la VICH). Se dirigen principalmente a la industria farmacéutica
indicando qué datos de validación deben proporcionarse en un expediente de solicitud. Estos datos deben demostrar que las pruebas y los criterios de aceptación propuestos están suficientemente controlados para garantizar una calidad reproducible de los productos en el momento de su comercialización y un control adecuado durante su vida útil (estabilidad).
Dado que las circunstancias en las que trabaja una OMCL son diferentes de las de una empresa farmacéutica – en la mayoría de los casos no se realizan análisis rutinarios, sino que a menudo las respuestas deben en un corto periodo de tiempo, es necesario reconsiderar el grado de validación/verificación antes de realizar un análisis. Por otra parte, en todos casos debe garantizarse que el resultado presentado es fiable. También hay que destacar que los materiales de referencia adecuados son un factor importante tanto para la realización de los los estudios de validación/verificación como en el propio análisis. El uso de preparados de referencia es ampliamente aceptado puede evitar en determinadas circunstancias la consideración de algunas
características de validación, sobre todo en el ámbito de los productos biológicos: esto debe justificarse caso por caso. El OMCL podrá decidir el alcance necesario teniendo en cuenta los factores de riesgo.
El ámbito de aplicación de este documento -dirigido específicamente a los OMCL- es orientar sobre el alcance de la validación/verificación necesaria, en función de diversas circunstancias, es decir, el objetivo del análisis (por ejemplo, detección de incumplimiento), la cantidad de datos de validación ya disponibles (por ejemplo, en caso de transferencia de un método), la experiencia o los datos históricos ya disponibles en el OMCL individual (por ejemplo, recuperación a partir de una matriz compleja; uso rutinario de una valoración estándar incluso si se valoran sustancias diferentes), etc.
Este documento es igualmente aplicable a productos de origen sintético y biológico. No aborda las prácticas habituales de laboratorio: por ejemplo, orientaciones relativas al uso del equipo, calibración, etc.
Este documento es una nota orientativa que ofrece recomendaciones detalladas sobre el de validación/verificación en función de la categoría del procedimiento analítico; cabe señalar que siempre son posibles otros enfoques. Con respecto a la nueva Directiva 2010/63/UE relativa a la utilización ética de los animales para fines científicos y educativos y el convenio europeo sobre protección de los animales vertebrados utilizados para experimentación y Otros Fines Científicos (Consejo de Europa) es necesario prestar especial atención al uso de métodos in vivo como procedimientos analíticos. Debe hacerse todo lo posible para racionalizar y racionalizar y restringir al mínimo necesario la utilización de animales sobre la base de un análisis exhaustivo de la situación.
Cabe destacar que este documento no puede ofrecer asesoramiento detallado para todos los casos posibles en los que se utilicen ensayos in vivo. El propósito de este documento es proporcionar una orientación general. En todos los casos, deberá incluirse una breve descripción y/o justificación del enfoque elegido, incluidos los métodos, deberá describirse en la documentación interna del análisis.
Datos de validación
Deberán justificarse las modificaciones del método validado original. En función de la naturaleza de las modificaciones y del resultado de la evaluación del riesgo, podrán emprenderse actividades de validación o verificación suplementarias. Se aplicarán las mismas definiciones que en el documento ICH.
Categorías de análisis
En este capítulo se definen las diferentes situaciones analíticas (categorías) que pueden darse en un OMCL y las características de validación correspondientes que deben tenerse en cuenta. Consulte la versión actual de la directriz ICH sobre «Validación de procedimientos analíticos»: Text and Methodology» (Q2).
Los estudios formales de validación, de acuerdo con los requisitos de la ICH, deben llevarse a cabo cuando se desarrolle un nuevo método, cuando se utilice un método existente o cuando los datos de validación de un método existente deban completarse.
Según la norma ISO 17025, la validación es necesaria para los métodos no normalizados. .En el contexto de la OMCL, los métodos de farmacopea y los métodos validados de una autorización de comercialización se consideran métodos estándar.
La verificación del método debe realizarse para demostrar que en las condiciones reales de uso en los laboratorios individuales el método (validado) es adecuado (apto para su uso). Esto puede lograrse realizando las pruebas de idoneidad del sistema (por ejemplo, la resolución en un método cromatográfico) el control de la sensibilidad en el umbral de notificación, el control de la integridad de un paso de reacción (por ejemplo, extracción, reacción de hidrólisis) antes de que pueda realizarse la determinación propiamente dicha, verificar la precisión del método, etc. Esto también puede lograrse realizando un ejercicio de transferencia del método, en el laboratorio que ha establecido el método y el OMCL y comparando los resultados para demostrar la equivalencia. En todos los casos, se incluirá una breve nota en la que se expliquen los motivos del método elegido (en función de la complejidad del análisis requerido). La complejidad del análisis requerido-, deberá incluirse en la documentación interna del análisis. Las desviaciones de esta directriz deberán justificarse.
En las tablas 1 a 8 se contemplan varias categorías de análisis:
Tabla 1: Método publicado en la Farmacopea Europea
Los procedimientos analíticos descritos en una monografía se consideran validados. El OMCL debe verificar que todos los materiales de referencia necesarios y que se realizan las pruebas de idoneidad del sistema requeridas. Para las pruebas de sustancias relacionadas, la especificidad para cualquier impureza conocida que no figure en la monografía (por ejemplo, la lista de transparencia Ph Eur). Para las monografías de productos terminados, el OMCL debe verificar que ningún excipiente interfiera en el análisis de la sustancia activa, a menos que se indique contrario en la monografía.
Nota: Para entrar en esta categoría, los procedimientos deben ser descritos en detalle, no por ejemplo como en algunos casos para biológicos donde hay sólo una descripción general del método. Los detalles pueden proceder del informe publicado del estudio colaborativo (por ejemplo, los informes de estudios BSP en Pharmeuropa Bio & Scientific notes)
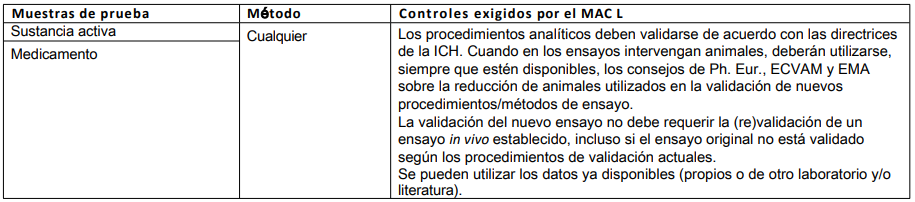
Tabla 2: Método validado de un fabricante (1ª autorización de comercialización)
Los procedimientos analíticos tomados de una autorización de comercialización están totalmente validados por la empresa.
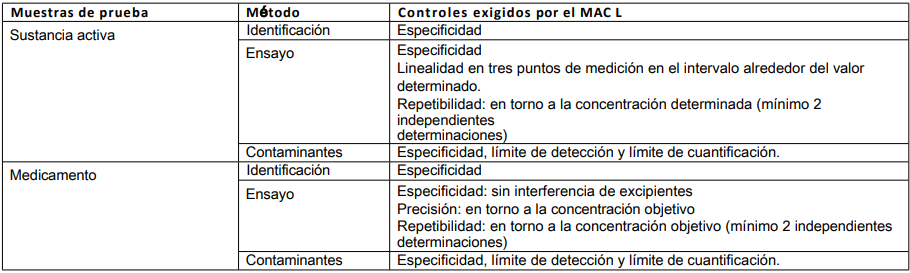
1er MAH = producto fabricado por el MAH que validó el método original utilizado. 2º HAC = producto de un fabricante diferente
para el que no se ha validado específicamente el método original utilizado.
Cuando los métodos procedan de un expediente o expedientes de solicitud antiguos sin datos de validación o con datos insuficientes, se deberá informar a la Autoridad Competente supervisora. Para las características de validación que deben tenerse en cuenta, véanse las tablas 2, 5.
Tabla 3: Método publicado no compendial
Las características de validación a considerar dependerán siempre de la cantidad de datos de validación aportados. Si el método ha sido completamente validado y los datos se han publicado en la bibliografía, véase el cuadro 1. En caso contrario, deberá tenerse en cuenta lo siguiente.
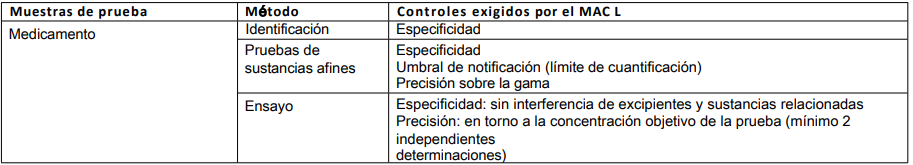
Tabla 4: Método de sustancia activa utilizado para un medicamento
El principal factor a considerar aquí es la influencia de la matriz en el análisis, incluyendo la interferencia de los excipientes.
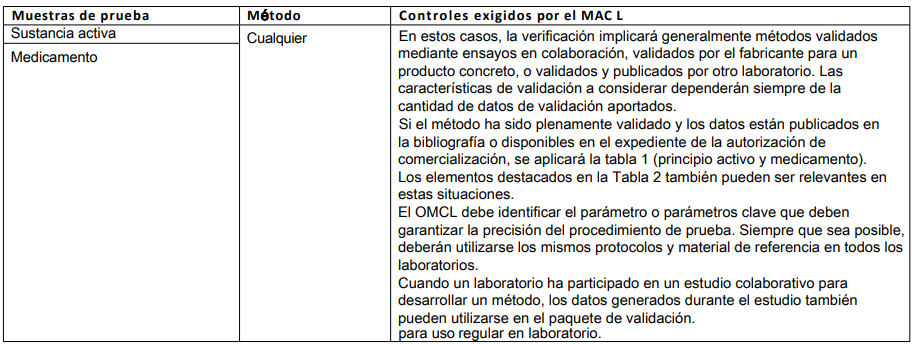
Tabla 5: Métodos validados para reducir, perfeccionar o sustituir el uso de animales (3R)
Tabla 6: Detección de incumplimientos
El cribado de la no conformidad significa que el objetivo del análisis es detectar la posible no conformidad del producto con las especificaciones.
Este tipo de cribado se realizaría cuando se solicita un análisis rápido y/o cuando no se dispone de datos de validación del método. El procedimiento debe documentarse en todos los casos.
Si se detecta un incumplimiento, debe ampliarse el alcance de la validación, por ejemplo, considerando la posibilidad de cambiar a un método bien reconocido (método de compendio o método del expediente MAH).
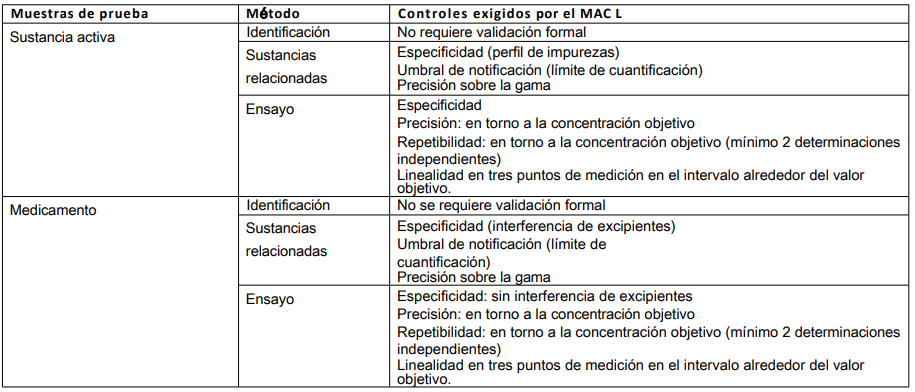
Tabla 7: Detección de productos/contaminantes desconocidos
En estos casos, se carece de información sobre el producto que debe analizarse con respecto a su declaración en la etiqueta (presencia o ausencia de determinadas sustancias) o para aclarar otros aspectos solicitados por la Inspección.
Pruebas a tener en cuenta: identificación, ensayo y, tal vez, pruebas de pureza. El primer paso importante es identificar los principales componentes del producto.
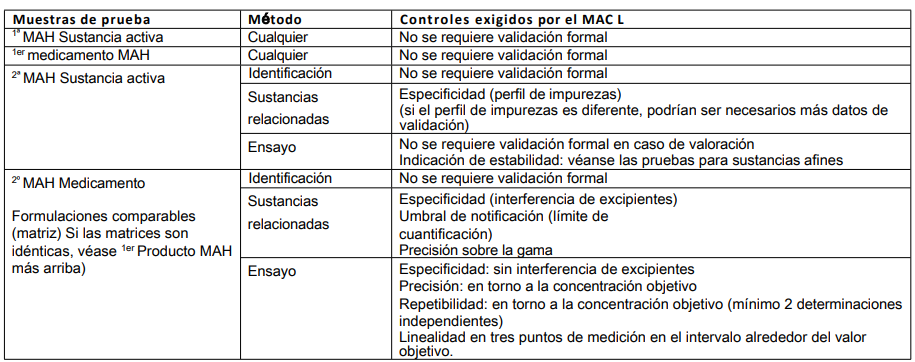
Tabla 8: Desarrollo de un nuevo método
Esto ocurre principalmente cuando un producto se prueba en condiciones de ensayo rutinarias y/o cuando se utiliza un procedimiento analítico interno.

¿Existen herramientas en el mercado que mejoren los procesos administrativos y de laboratorio?
Como bien sabemos el desafío más grande al que se a puesto a prueba el sector farmacéutico es el relacionado con la integridad de datos. Y el proceso de validación de método analíticos no cae fuera de este requerimiento ¡Pero! ¿Por qué es tan complejo este tema? La respuesta se deriva por la gran cantidad de datos y documentos que se emiten día con día en el que se ven impactados documentos y libros de Excel.
Recordemos que la validación de software y libros de Excel es el primer paso. No obstante, muchos libros de Excel utilizados en el sector farmacéutico no cuentan con evidencia de validación lo cual es un riesgo que podrá derivar en un hallazgo critico ante una inspección regulatoria.
El segundo paso y el más complejo es adherir las configuraciones necesarias que eleven la integridad de datos y favorezcan el mantenimiento tanto de software como de Libros de Excel.
Te invitamos a mitigar el riesgo por el uso de sistemas computarizados no validados y con pobres atributos de integridad de datos. Nuestros desarrollos están estructurados bajo un sistema de gestión de calidad trazable y auditable. Tales cuales cuentan con el soporte de validación-calificación documental con base en Gamp 5 y CFR21 parte 11.
Conoce eADMxL el cual es un software que desarrollamos para mitigar el uso de hojas de cálculo para procesos de validación de métodos analíticos. Conoce sus beneficios y alcance general aquí: ¡Da clic aquí!
“No vivas con el riesgo ¡Mitígalo!” para eso nosotros de ayudamos.
Visita nuestro sitio www.deappharma.com y solicita una demostración y asesoría gratuita.
¡Contáctanos! y conoce de que manera te vamos a ayudar.
¡Únete a nuestra comunidad en redes!
Referencias
- General European OMC L Network (GEON) Quality Management Document
- Validation of analitycal procedures :text and methodology Q2
12, Abr 2023
Definiendo los requerimientos de usuario
Una clave muy importante para la validación del software y libros de Excel es una especificación documentada de los requisitos que defina:
– el «uso previsto» del software, libro de Excel o equipo automatizado; y
– la medida en que el fabricante del producto depende de ese software, libro de Excel o equipo para la producción de un producto sanitario de calidad.
El fabricante del producto (usuario) tiene que definir el entorno operativo previsto, incluyendo cualquier configuración de hardware y software necesarias, versiones de software, utilidades, etc. El usuario también debe:
– documentar los requisitos de rendimiento del sistema, calidad, gestión de errores, puesta en marcha, apagado, seguridad, etc;
– identificar cualquier función o característica relacionada con la seguridad, como sensores, alarmas, enclavamientos, pasos lógicos de procesamiento o secuencias de comandos; y
– definir criterios objetivos para determinar el rendimiento aceptable.
La validación debe realizarse de acuerdo con un protocolo documentado, y los resultados de la validación también deben documentarse. Deben documentarse los casos de prueba que pongan a prueba el rendimiento del sistema con respecto a los criterios predeterminados, especialmente para sus parámetros más críticos.
Los casos de prueba deben abordar las condiciones de error y alarma, el arranque, el apagado, todas las funciones de usuario y controles de operador aplicables, posibles errores de operador de valores permitidos y las condiciones de estrés aplicables al uso previsto del equipo. Los casos de prueba deben ejecutarse y los resultados deben registrarse y evaluarse para determinar si los resultados permiten concluir que el programa informático está validado para el uso previsto.
Un fabricante de productos puede llevar a cabo una validación utilizando su propio personal o puede depender de un tercero, como el fabricante del equipo/software tercero, o un consultor. En cualquier caso, el fabricante del producto conserva la responsabilidad última de garantizar que el software del sistema de producción y calidad:
– se valide de acuerdo con un procedimiento escrito para el uso concreto previsto; y
– funcionará según lo previsto en la aplicación elegida.
El fabricante del producto debe disponer de documentación que incluya
– los requisitos de usuario definidos
– el protocolo de validación utilizado
– los criterios de aceptación
– casos de prueba y resultados; y
– un resumen de validación que confirme objetivamente que el software y/o Libros de Excel está validado para el uso previsto.
¿Existen herramientas en el mercado que mejoren los procesos administrativos y de laboratorio?
Como bien sabemos el desafío más grande al que se a puesto a prueba el sector farmacéutico es el relacionado con la integridad de datos. ¡Pero! ¿Por qué es tan complejo este tema? La respuesta se deriva por la gran cantidad de datos y documentos que se emiten día con día en el que se ven impactados documentos y libros de Excel.
Recordemos que la validación de software y libros de Excel es el primer paso. No obstante, muchos libros de Excel utilizados en el sector farmacéutico no cuentan con evidencia de validación lo cual es un riesgo que podrá derivar en un hallazgo critico ante una inspección regulatoria.
El segundo paso y el más complejo es adherir las configuraciones necesarias que eleven la integridad de datos y favorezcan el mantenimiento tanto de software como de Libros de Excel.
Te invitamos a mitigar el riesgo por el uso de sistemas computarizados no validados y con pobres atributos de integridad de datos. Nuestros desarrollos están estructurados bajo un sistema de gestión de calidad trazable y auditable. Tales cuales cuentan con el soporte de validación-calificación documental con base en Gamp 5 y CFR21 parte 11.
Conoce eADMxL el cual es un software que desarrollamos para mitigar el uso de hojas de cálculo para procesos de validación de métodos analíticos. Conoce sus beneficios y alcance general aquí: ¡Da clic aquí!
eDocuSeed es más que un software de gestión documental ya que este es capaz de controlar y mantener libros de Excel por medio de adición de controles necesarios para: acceso, edición, trazabilidad y su mantenimiento. Conoce sus beneficios y alcance general aquí: ¡Da clic aquí!
“No vivas con el riesgo ¡Mitígalo!” para eso nosotros de ayudamos.
Visita nuestro sitio www.deappharma.com y solicita una demostración y asesoría gratuita.
¡Contáctanos! y conoce de que manera te vamos a ayudar.
¡Únete a nuestra comunidad en redes!
6, Mar 2023
Importancia de la integridad de datos en procesos de validación de métodos analíticos
La integridad de datos es un aspecto crucial en el proceso de validación de métodos analíticos en la industria farmacéutica. La validación de métodos analíticos es un proceso que asegura que un método analítico específico es adecuado para su uso previsto y que proporciona resultados precisos y confiables.
La integridad de los datos es esencial en la validación de métodos analíticos porque los datos generados durante el proceso de validación se utilizan para establecer la precisión, la exactitud, la linealidad, la especificidad y la robustez del método analítico. La falta de integridad de los datos puede comprometer la precisión y confiabilidad de los resultados y poner en riesgo la seguridad y eficacia de los productos farmacéuticos.
Además, las autoridades reguladoras exigen que los datos utilizados en la validación de métodos analíticos sean precisos, confiables y completos. La falta de integridad de los datos puede poner en duda la validez de los resultados de la validación y poner en riesgo la aprobación de los productos.
Por lo tanto, la integridad de los datos es fundamental en el proceso de validación de métodos analíticos y se deben implementar controles rigurosos para garantizar que los datos generados durante el proceso de validación sean precisos, confiables y completos. Esto incluye la capacitación del personal, la implementación de controles de acceso y seguridad, la validación de sistemas, la verificación de datos y la revisión regular de la documentación y registros.
¿Cuales son los 5 hallazgos de integridad de datos en Hojas de cálculo en el sector farmacéutico?
A continuación de algunos hallazgos comunes de integridad de datos que se han observado en hojas de cálculo en sectores regulados, incluido el farmacéutico:
- Errores de entrada de datos: Los errores de entrada de datos son comunes en las hojas de cálculo y pueden deberse a errores humanos al ingresar información. Estos errores pueden incluir errores tipográficos, errores de transposición o errores de formato.
- Fórmulas incorrectas: Las fórmulas incorrectas pueden llevar a resultados inexactos y pueden deberse a una variedad de factores, como errores humanos, cambios en los datos de origen y copiar y pegar incorrectos.
- Control de cambios insuficiente: La falta de control de cambios puede hacer que sea difícil realizar un seguimiento de los cambios realizados en una hoja de cálculo y puede dificultar la identificación de errores o fraudes.
- Falta de validación de datos: La falta de validación de datos puede hacer que los datos sean inexactos o incompletos. Esto puede incluir la falta de validación de datos de entrada o la falta de validación de datos calculados por fórmulas.
- Falta de documentación: La falta de documentación puede dificultar la comprensión de cómo se creó una hoja de cálculo, lo que puede hacer que sea difícil identificar errores o fraudes. Es importante mantener una documentación completa y actualizada de las hojas de cálculo para garantizar la integridad de los datos.
Ahora que conoces la importancia de la integridad de datos en el proceso de validación de métodos analíticos y los hallazgos recurrentes en la industria vamos con el siguiente paso ¡Mejorar el proceso! ¿Quieres saber como?
¡DA CLIC AQUI!

¡Contáctanos! y conoce de que manera te vamos a ayudar.
¡Únete a nuestra comunidad en redes!
24, Nov 2022
Registros electrónicos (Identificadores)
Cuando se gestionan documentos o datos de laboratorio dentro de la industria regulada una función importante dentro del entorno de las buenas prácticas de laboratorio en sistemas computarizados e informatizados es aquel relacionado al control de registros. Visto desde una parte de trazabilidad este identificador es la base de búsqueda de algún documento y/o el comienzo para vincular acciones preestablecidas ya que es de carácter único.
Este articulo estará enfocado hacia el proceso de validación de métodos analíticos, sin embargo el concepto general aplica a diferentes esquemas de software eg, sistemas documentales, datos de laboratorio y hojas de cálculo.
Para comenzar con este articulo compartimos las siguientes definiciones, tales cuales anteceden la esencia de estas líneas.
Como definiciones para el proceso de validación de métodos analíticos establecidas por FDA y USP, respectivamente son;
FDA: “La validación de un método analítico es el proceso por el cual se establece, mediante estudios de laboratorio, que las características de desempeño del método cumplen con los requisitos para las aplicaciones analíticas previstas.”
USP: “La validación de métodos, es el proceso por el cual se demuestra que los procedimientos analíticos son aptos para el uso indicado.”
Como se puede percibir en las definiciones anteriores sobre la validación de métodos analíticos, se haca referencia a la palabra “PROCESO”. La definición de proceso se expresa de la siguiente manera: procesamiento o conjunto de operaciones a que se somete una cosa para elaborarla o transformarla.
Como bien sabemos los procesos de validación de métodos analíticos actualmente son realizados con el uso de hojas de cálculo, donde podemos encontrar varios gaps de integridad de datos. Bajo esta situación el control de registros depende de la clave que se asigna al protocolo de validación correspondiente y por ende el sitio donde se almacena la carpeta física con resultados.
Durante nuestra experiencia hemos observado diferentes situaciones desafortunadas para acceder a la información con procesos de gestión actual, los más representativos son:
- La información no se encuentra en el sitio ubicado destinado en el archivo muerto.
- La información impresa se extrajo y nunca se regresó a su sitio.
- La información impresa se puede destruir y generar un reporte nuevo sin posibilidad de trazar la existencia del primer documento.
Derivado de las situaciones anteriores no solo se observa un impacto sobre los documentos y/o datos de laboratorio. Lo que se impacta de manera esencial es la integridad de los datos y la toma de decisiones.
¿Cómo se impacta la integridad?
La integridad se ve impactada por la falta de control sobre datos y registros. Recordemos que la integridad de datos define que los datos y documentos deben ser perdurables para que estos se mantengan: atribuibles, legibles, contemporáneos y exactos. Por ende, la manera actual de gestionar las validaciones carece de integridad con grandes áreas de oportunidad que se deben atender y solucionar.
¿Que son los registros?
Una parte importante para el control de datos es la estructuración sistemática de registros, tales cuales deben ser ordenados y monitorizados. Pero ¿Qué es un registro?
Un registro es toda la información de un elemento que se almacena en un archivo o tabla de base de datos; por ejemplo, el conjunto de datos debe incluir el nombre del producto, tipo de trabajo, dosis, categoría de método a evaluar, tipo de prueba, referencias de protocolos y vigencias. Así como quien y cuando se creó dicho registro. En algunos casos específicos un registro debe permitir la correlación de este con otros previamente realizados.
Como se mencionó los registros son identificadores únicos tales cuales están estructurados por prefijos, sufijos y números establecidos por algoritmos establecidos. De esta manera se da una secuencia definida sin posibilidad de duplicidad y con una completa trazabilidad mediante pistas de auditoría. Es importante considerar que los registros dentro de los sistemas computarizados e informatizados deben ser ordenados e identificados de manera secuencial para una búsqueda eficiente y un acceso rápido.
¿Nosotros como lo hacemos?
A continuación, te mostramos la secuencia de pasos que realiza nuestro sistema estrella para la creación, control y acceso a registros de validación de métodos analíticos. No obstante, te invitamos a revisar nuestros otros desarrollos, tales cuales cuentan también con estas funciones.
Vallamos entonces.
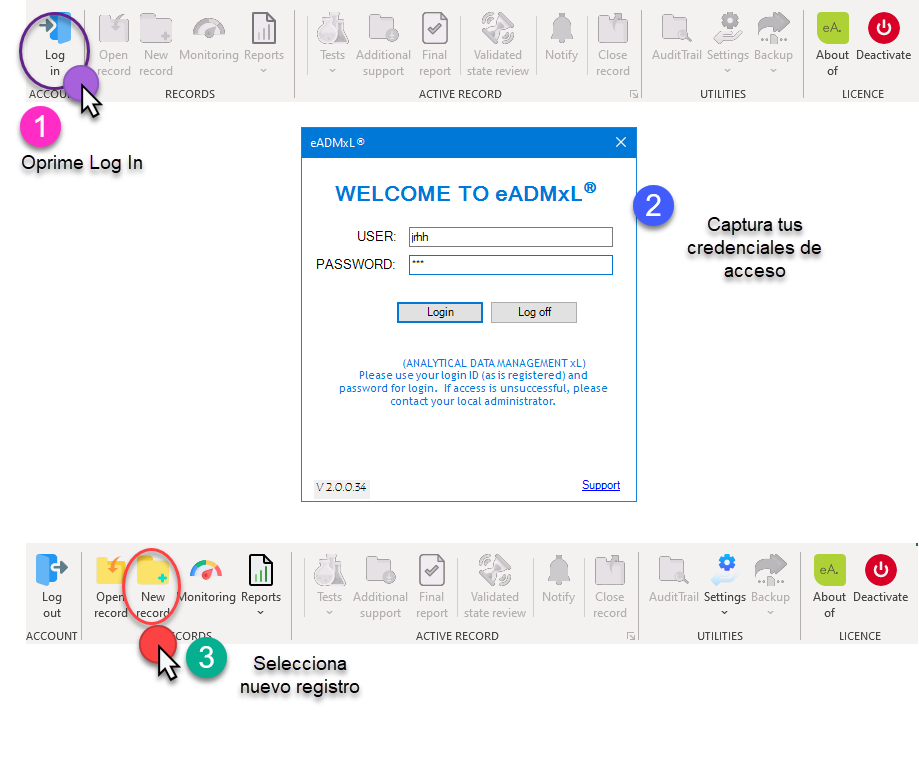
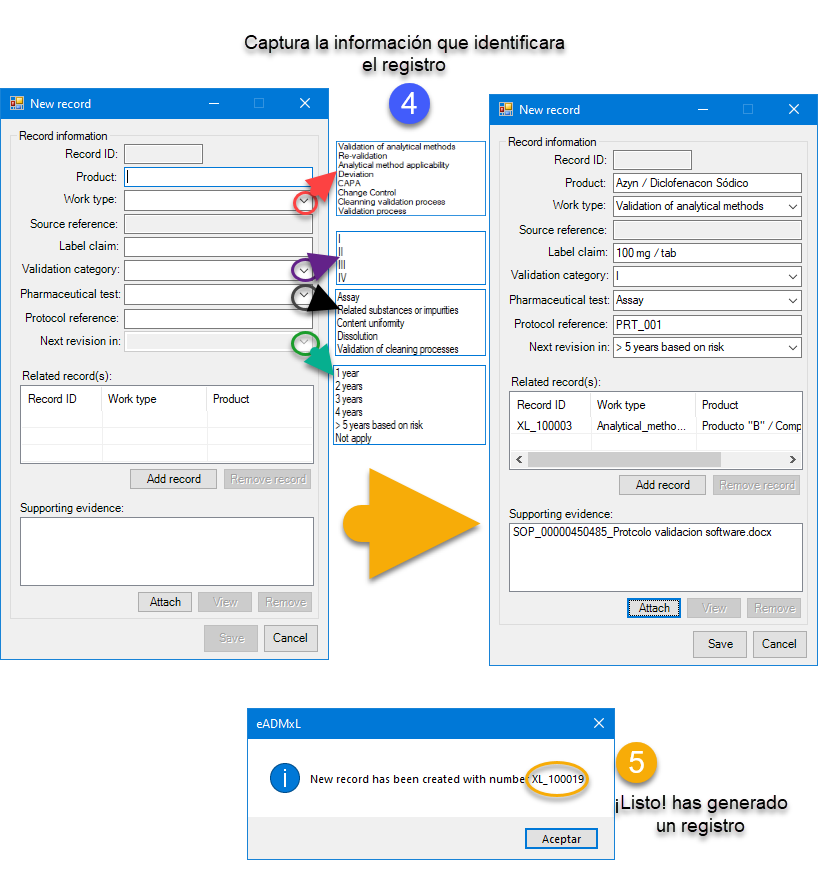
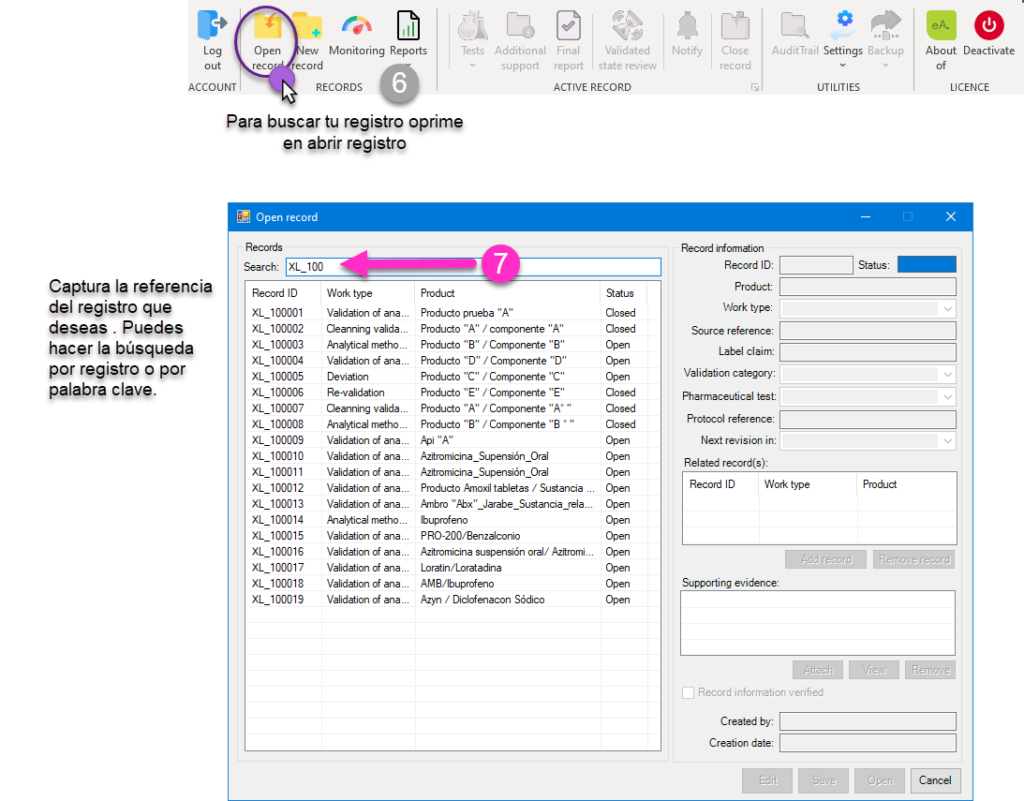
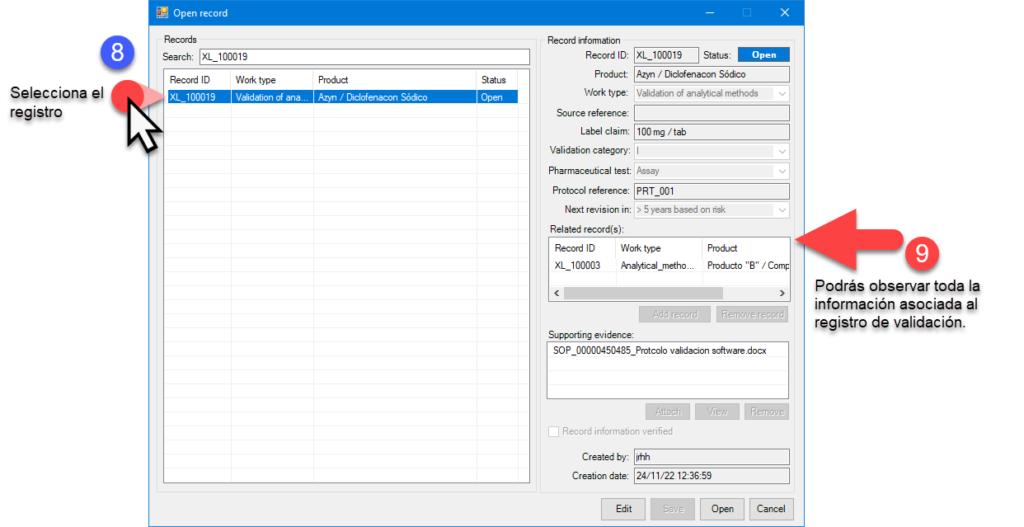
En la actualidad hay muchos gaps relacionados al acceso y control de sistemas computarizados (se incluyen hojas de cálculo). Es por esto que en deappharma desarrollamos herramientas que potencian tu cumplimiento de manera fácil y lógica. Te invitamos a conocer y solicitar tu DEMO y/o implementación de licencia gratuita de nuestro sistema estrella eADMxL para realizar el proceso de validación de métodos analíticos. También te invitamos a explorar nuestros otros desarrollos y visualizar en que proceso te podemos ayudar.
El cambio está en tus manos. Nosotros de ayudamos a potenciar tu cumplimiento.
Referencias:
- FDA draft guidance – Analytical Procedures and Methods Validation
- USP 31 –NF 26, Capítulo General Validación de métodos farmacopéicos
- Villareal de la Garza Sonia, Introducción a la computación. Cap 8 Ed. McGrawHill , México , 2007
¿Necesitas ayuda?
¡Contáctanos! y conoce de que manera te vamos a ayudar.
¡Únete a nuestra comunidad en redes!
5, Sep 2022
¿Qué debo saber para abordar la Validación de hojas de cálculo?
Las hojas de cálculo también llamadas planillas, templetes, plantillas de cálculo, son herramientas rutinariamente utilizadas para realizar actividades GxP de carácter normativo. Es por esto que el control y el uso de estas debe ser regulado derivado de que pueden tener impacto sobre la exactitud, fiabilidad, integridad, disponibilidad, autenticidad de los registros y firmas requeridas, según aplique.
Para poder comprender la criticidad e importancia de la emisión de datos con estas herramientas, podríamos partir respondiendo a las siguientes preguntas; ¿Cuál es el objetivo de validar una hoja de cálculo? ¿Qué hace tan viable el uso de las hojas de cálculo como una herramienta en entornos GxP? ¿Qué debo saber antes de comenzar una validación de hoja de cálculo? ¿Cómo definir el alcance de validación de una hoja de cálculo? O más aún ¿Podría auto inspeccionar mi hoja de cálculo? Las respuestas a las preguntas antes mencionadas nos brindan un panorama general de conocimiento.
¿Cuál es el objetivo de validar una hoja de cálculo?
El objetivo de validación de una hoja de cálculo nos encanta definirlo de la siguiente manera: “Buscar la verdad de algo”. Para lo cual debemos revisar, auditar y documentar que una hoja de cálculo emite resultados fidedignos respecto a la especificación de requisitos establecida.
¿Qué hace tan viable el uso de las hojas de cálculo como una herramienta en entornos GxP?
En entornos Gxp se genera una gran cantidad de data que va desde lo simple, lo que podemos denominar texto o escritura hasta data compleja, tendencias, inferencias, decisiones etc. es aquí donde las hojas de cálculo adquieren relevancia ya que estas otorgan al usuario versatilidad, dinamismo y poder de personalización que va desde la vinculación de celdas configurables, hasta la creación de código VBA o MACROS personalizados.
¿Qué debo saber antes de comenzar una validación de hoja de cálculo?
Antes de comenzar una validación de hoja de cálculo es necesario evaluar de manera documentada la hoja de cálculo, es decir definir el riesgo y la expectativa de validación. Una excelente manera para definir es aquella que se relaciona a la complejidad. En función de la complejidad de la hoja de cálculo los resultados requeridos son escalables. Aquí un ejemplo para definir complejidad dentro de este rubro:
- Simple: la hoja de cálculo se considera simple cuando utiliza funciones estándar de Excel. Se pueden utilizar cálculos y otras funciones de Excel (formulas) sencillas siempre que los requisitos estén documentados con suficiente detalle para permitir la realización de pruebas GxP. Si un cálculo o una fórmula no se expresa o no puede expresarse suficientemente en los requisitos, la hoja de cálculo debe considerarse compleja y debe generarse una especificación de diseño.
- Compleja: la hoja de cálculo se considera compleja cuando utiliza funciones no estándar de Excel, como objetos personalizados, macros o Visual Basic. Una hoja también se considera compleja si un cálculo o una fórmula utilizada no se expresa o no pueden expresarse suficientemente en los requisitos indicados anteriormente. Si la hoja de cálculo contiene una amplia codificación personalizada, no debe validarse siguiendo estándares de validación de hojas de cálculo. Es grado de personalización deberá trabajarse como una validación de software utilizado criterios y parámetros de validación diferentes.
¿Cómo definir el alcance de validación de una hoja de cálculo?
El alcance de validación se define con base en la complejidad. Y con base en esta complejidad se define el entregable, un alcance típico es el siguiente:

¿Podría auto inspeccionar mi hoja de cálculo?
La regulación no establece limitantes para que puedas ser tu mismo quien valide tu hoja de cálculo. Sin embargo, se sugiere que la validación sea llevada por un ente ajeno a tu proceso. De esta manera la validación y auditoria de la hoja de cálculo podrá ser realizada de manera objetiva.
Expertos en Validación de Hojas de Cálculo de Microsoft Excel
No olvides que en caso de ser necesario, puedes contactarnos para mejorar el proceso de laboratorio y/o administrativo de tu organización a través software 100% confiable y seguro.
Recuerda que en deappharma contamos con un software que te ayudara a administrar y controlar tu proceso de libros y hojas de Excel. Somos expertos en la materia, por lo que procesos complejos no representa un reto para nosotros, debido a que tenemos en mente los aspectos relevantes de cumplimiento.
Te invitamos a adquirir nuestro servicio de validación, auditoria o diseño de hojas de cálculo y no te pierdas del beneficio extra que tenemos para ti. Conoce este beneficio ¡da clic aquí!
Contáctanos en: info@deappharma.com
¡Únete a nuestra comunidad en redes!
27, Jun 2022
Validación de hojas y libros de Excel
Validación de Hojas de Cálculo de Microsoft Excel
Te has preguntado si validar una hoja de Excel es equivalente a contar con una hoja de Excel integra. Aunque los conceptos parecen a simple vista los mismos. Es una realidad que no. Pero para comprender esto partamos de lo siguiente
Una hoja de cálculo es una estructura tabular de renglones y columnas que permiten realizar operaciones matemáticas, procesar números y ayudar a realizar cálculos desde los más simples hasta los más complejos que implican manipular muchos números y realizar muchas operaciones numéricas.
La importancia de validar una hoja de cálculo Excel reside en que estas pueden afectar directa o indirectamente los atributos de calidad de los productos o procesos. Así como ayudar a una toma de decisión como, por ejemplo: la aprobación de un lote producto para su venta.
La validación de hojas de cálculo Excel no cae fuera de la definición que se establece en la normatividad local e internacional para validación. Existen diversas definiciones de validación, sin embargo, las más completas y consistentes son las de la NOM-059-SSA y la de la FDA, que la definen como:
NOM-059-SSA
<<…”es la evidencia documentada que demuestra que a través de un proceso especifico se obtiene un producto que cumple consistentemente con las especificaciones de calidad establecidas.” …>>
FDA
<<…” el establecimiento de evidencia documentada que proporciona un alto grado de seguridad, que un proceso especifico produce consistentemente sus especificaciones predeterminadas y sus atributos de calidad.” …>>
En donde:
- Documentada. La validación requiere de una minuciosa documentación de todas las acciones que se lleven a cabo dese el inicio hasta el final del estudio.
- Alto grado de seguridad y confianza. Se asume que incluso un programa grande en un sistema complejo computarizado se encuentra realmente libre de errores.
- Proceso especifico. Toda la validación de una hoja de cálculo es un proceso. Por ejemplo, el desarrollo y actividades de prueba de la hoja de cálculo son validadas para asegurar el buen funcionamiento de la hoja de cálculo. Algunas subpartes de validación, tales como calificaciones (instalaciones, operación y desempeño) son especificaciones para cada sistema.
- Consistente. La validación no es un evento de una sola ocasión. El desempeño del sistema de cómputo tiene que ser controlado durante el tiempo de vida del producto.
- Especificaciones. Las actividades de validación comienzan con la definición de especificaciones. El desempeño del sistema de cómputo tiene que ser verificado contra esas especificaciones. El criterio de aceptación está definido por esta prueba.
Enfoque para las hojas de cálculo (Excel) en concordancia con CFR21 parte 11 como sistema cerrado
Las hojas de cálculo Excel son considerados registros electrónicos, por este hecho deben ser tratadas como un sistema informatizado.
Un registro electrónico considera, los documentos y registros que son creados, modificados, mantenidos, archivados, recuperados y/o transmitidos a través de sistemas electrónicos.
Cuando se utilicen sistemas electrónicos para la creación, modificación, mantenimiento, archivo, recuperación y/o transmisión de registros electrónicos deberán establecer procedimientos y controles diseñados para asegurar la autenticidad, integridad y cuando aplique confidencialidad de los registros electrónicos y para asegurar que las firmas electrónicas no puedan ser declaradas como no genuinas. Los procedimientos y controles deben incluir:
- La validación de los sistemas para asegurar la exactitud, confiabilidad, funcionalidad, consistencia y la habilidad para distinguir entre registros inválidos o alterados.
- La habilidad de los sistemas o aplicaciones computacionales para generar copias de los registros exactas y completas, legibles tanto en su versión manual como electrónica, que permitan su inspección, revisión y copia.
- La protección de los registros, que permita su recuperación en forma rápida y exacta durante todo el periodo de conservación de estos.
- El permitir el acceso al sistema únicamente a personas autorizadas.
- El uso de los procesos de auditoría de rastreo seguros, generados por computadora, para registrar en forma independiente el acceso al sistema, así como las acciones que creen, modifiquen o borren registros electrónicos.
- Cotejos operacionales del sistema para obligar que los pasos y eventos ocurran en la secuencia establecida.
- Los cotejos para asegurar que solamente personas autorizadas puedan utilizar el sistema, firmar electrónicamente un registro, acceder a la operación del dispositivo de entrada y salida del sistema computarizado, modificar un registro o realizar la operación manual.
- La determinación de que las personas que desarrollan mantienen o utilizan sistemas de firmas/registros electrónicos tienen la capacidad, adiestramiento y experiencia para llevar a cabo sus tareas.
Firmas electrónicas
Las firmas electrónicas son una compilación de datos en la computadora ejecutados para algunos símbolos, adoptados o autorizados por un individuo que son equivalentes a su firma manuscrita. Para el caso de firmas electrónicas se debe considerar:
- Debe contener la información asociada con la firma que claramente indiquen el nombre en letra de molde de la persona que forma, la fecha y hora de cuando fue ejecutada la firma y el propósito asociado con la misma.
- Estas deben ser únicas para cada persona y cuando se dé el caso de un cambio, esta no debe repetirse o reasignarse a otra persona.
- Cuando el uso de las firmas electrónicas sea adoptado, se debe establecer la fecha a partir de la cual las firmas electrónicas son vigentes y equivalentes a las firmas en manuscrito, para lo cual es necesaria una certificación en un forma u hoja de papel y firmada con una firma en manuscrito.
Que debemos considerar al validar hojas de cálculo (Excel)
Como hemos descrito anteriormente las hojas de cálculo de Excel son consideradas sistemas computarizados. ¿Pero que hay acerca del proceso de validación?
Antes de comenzar debemos conocer y/o actualizar el plan maestro de validación, ya que en este documento deberemos describir por lo menos lo siguiente:
- Nombre del archivo de la hoja de cálculo incluyendo el número de versión
- Ubicación y lugar de almacenamiento de la hoja de cálculo
- Sistema operativo y Software utilizado (resumen de las instalaciones, sistemas, equipos y procesos a evaluar.
Para comenzar debemos partir de dos supuestos que serán los que necesitamos para alcanzar el objetivo. Obtener certidumbre sobre la integridad de datos de las hojas de cálculo Excel es un proceso que se debe llevar de manera sinérgica. Con esto el control y trazabilidad se otorga mediante soluciones informáticas que eleven sustancialmente el control y administración de nuestros libros de Excel que están validados y auditados de manera adecuada. Compartimos contigo lo siguiente para llevar a cabo el proceso de calificación/validación de libros de Excel.
Antes de iniciar con la validación de la hoja de cálculo de Excel debemos establecer los requerimientos de usuario de dicho libro. Recuerda que los requerimientos de usuario establecen de manera generar el alcance que tendrá el libro, sin describir de manera detallada el proceso de diseño y funcionalidad inicial.
Una vez establecidos los requerimientos de usuario del libro de Excel, podemos comenzar con el diseño de la hoja. De tal manera que desarrollemos la estructura de esta lo más acorde a lo establecido.
No obstante, también es factible desarrollar primero el libro y después estructurar los requerimientos de usuario. Esta opción favorece la redacción del documento de especificación.
El diseño de la hoja es una de las etapas más sensibles, ya que el formato y vinculación de cálculos se establece de manera sistemática y con escrutinio. Sin embargo, la verificación, validación y auditoria debe hacerse por un área ajena no dueña del Libro (recomendable).
Una vez se cuente con el desarrollo y diseño del libro de Excel viene la tarea de calificar/validar y auditar el archivo. Las consideraciones que deben formar parte de la documentación de soporte de validación son:
- Evaluación de precedencias. Esta evaluación indica el orden en que se ejecutan los cálculos en una fórmula si esta contiene varios operadores.
- Evaluación de celdas precedentes y celdas dependientes. Las celdas precedentes son aquellas que se refieren a fórmulas de otras celdas. Por otro lado, las celdas dependientes son aquellas que contienen fórmulas que se refieren a otras celdas.
- Referencias circulares. Este término se refiere al hecho de que una fórmula utilice la celda que lo contine como uno de sus parámetros de forma directa o indirectamente.
- Control de cálculo. Por defecto, Excel recalcula toda la hoja de cálculo cuando introduce un cambio en alguna de sus celdas.
- Inspección. La ventana de inspección es una función que forma parte de la auditoria de fórmulas de Excel. Con ella es posible visualizar la fórmula o las fórmulas de una misma hoja de cálculo de modo completo con el fin de facilitar su revisión, control y confirmación.
- Comprobación de errores. Se utiliza para localizar e identificar errores que pueden cometerse al introducir fórmulas.
- Revisión de ortografía. Se utiliza para corregir los textos contenidos dentro de los textos existentes en la hoja de Excel.
- Protección de la hoja. Existen diferentes herramientas en Excel para impedir que un usuario modifique, mueva o elimine accidental o premeditadamente los datos contenidos en las celdas de una hoja de cálculo o libro.
- Protección de la estructura del libro. Esta función impide la modificación de toda la estructura del libro, es decir, no permite mover, eliminar o agregar hojas, modificar su nombre, cambiar el tamaño de las ventanas, etc.
- Conservación. Esta función permite migrar un libro u hoja de Excel respectivamente hacia un sistema de alto control para su administración.
- Acceso seguro a libros de Excel. Esta función permite acceder de manera controlada al libro de Excel.
- Control de versiones. Esta función permite contralar mediante un explorador virtual las versiones de libros y hojas de cálculo.
- Pistas de Auditoria. Esta función permite establecer mediante un control de programación la estructuración dinámica de un “Audit Trail” sobre uso de cierto libro de Excel y su versión.
- Respaldo y Restauración. Esta función permite establecer la posibilidad de respaldar todos los archivos (libros de Excel) contenidos en la carpeta virtual.
Como lo has podido percibir, el alcanzar una hoja o libro de Excel con atributos de integridad de datos se vincula de estrechamente entre los controles “per se” de Excel y la sinergia con software de gestión y control.
Recuerda que en deappharma contamos con una herramienta que te ayudara a administrar y controlar atributos de tus hojas y/o libros de Excel para obtener un optimo desempeño de integridad y cumplimiento.
Beneficios de la validación de hojas de cálculo
Validar, administrar y controlar las hojas de cálculo o libros de Excel permite a las organizaciones:
- Permite mitigar uno de los riesgos más significativos en la industria. Siendo este la pobre integridad de las hojas de cálculo y su control.
- Los recursos físicos son optimizados como consecuencia del protagonismo digital. Así, el escaneo de los documentos físicos hace posible una reducción del tamaño de las instalaciones reservadas al archivo y custodia de todos los libros de Excel de la compañía.
- Centralización de la información, gracias a la cual se potencia tanto el flujo de trabajo como la colaboración entre distintos departamentos y, algo muy importante, entre distintas sedes o lugares de trabajo separados entre sí.
- Mayor grado de control de los diferentes libros gracias a la monitorización del ciclo de vida del archivo.
- Mayor seguridad, pues las copias de seguridad evitarán la destrucción de los libros, así como también se puede llevar un control sobre quién accede a los distintos libros y quién modifica la estructura de estos. Por lo que la sustracción de información sensible puede ser fácilmente rastreable.
Expertos en Validación de Hojas de Cálculo de Microsoft Excel
No olvides que, en caso de ser necesario, puedes contactarnos para mejorar el proceso de laboratorio y administrativo de tu organización a través software 100% confiable y seguro. Recuerda que en deappharma contamos con un software que te ayudara a administrar y controlar tu proceso de libros y hojas de Excel. Somos expertos en la materia, por lo que procesos complejos no representa un reto para nosotros, debido a que tenemos en mente los aspectos relevantes de cumplimiento.
Al mandar con nosotros tus libros y Hojas de Excel para validar, diseñar o auditar obtendrás nuestro software eDocuSeed de manera gratuita por un año. Conoce los beneficios de nuestro aplicativo ¡Da clic aquí!.
También te pueden interesar los siguientes artículos ¡Da clic en alguno de ellos!
Categorización de hojas de cálculo
Tipificación de hojas de cálculo
¡Contáctanos! y conoce de que manera te vamos a ayudar.
¡Únete a nuestra comunidad en redes!
11, Feb 2022
Audit Trail para asegurar y elevar el proceso de Integridad de datos
Este término regulatorio e informático se refiere a la auditoría, detección continua y exhaustiva de los datos. Por lo que es relevante contar con este proceso o función en cada uno de nuestros sistemas informatizados. El objetivo, es trazar la vida de un dato de manera perdurable.
La industria farmacéutica, dispositivos médicos y almacenes utilizan sistemas informatizados dentro de sus procesos. Por este hecho, es relevante el control y trazabilidad de datos. Para abordar el tema y conocer el alcance e importancia de la función de pistas de auditoria te invitamos a leer lo siguiente.
¿Qué es un “pista de auditoría”?
La «Pista de auditoría» o también conocida como «Audit Trail». Significa un registro electrónico seguro, generado por computadora con sellos de tiempo que permiten la reconstrucción del curso de los eventos relacionados con la creación, modificación y/o eliminación de un registro electrónico. Por ejemplo, la pista de auditoría para una ejecución de cálculos analíticos con la utilización de Excel como software de cálculo, debe incluir como mínimo lo siguiente: nombre de usuario, la fecha/hora de la ejecución, los cambios realizados sobre un valor y los detalles justificados de dicho cambio, según apliquen. ¡Pero no solo eso! Las pistas de auditoria son un aparte esencial de los sistemas computarizados. Es por esto, que los reportes de auditorita deben ser robustos y seguros.
Retomemos el ejemplo de uso de la hoja de Excel para obtención de resultados analíticos. En la actualidad la industria configura la obtención de pistas de auditoría sobre los mismos libros de Excel. Esta pista «LOG» regularmente la establecen dentro del mismo libro de manera anidada como una pestaña (hoja) de cálculo. ¡Esta práctica, es poco sostenible y segura! ya que la trazabilidad la dejas en manos de Excel y de la vulnerabilidad de código realizado con VBA.
¿Existe riesgo de perder la trazabilidad en mis libros de Excel por usar configuración VBA?
La respuesta es ¡Si! y tu impacto será alto porque no tendrás la manera de trazar la información.
Los riesgos los podemos clasificar en dos escenarios posibles:
- Daño en el archivo de Excel que no permita acceder a la información.
- Alteración y vulnerabilidad de la programación en VBA (Hasta videos en youtube te enseñan a desbloquear código relizadoo con VBA. ¡Ojo con esto!)
¿Quién debe revisar los registros de auditoría?
La revisión de la pista de auditoría es similar a la evaluación de las tachaduras en papel al revisar los datos. Personal responsable de la revisión de registros bajo cGMP debe revisar las pistas de auditoría que capturan los cambios en datos asociados con el registro a medida que revisan el resto del registro. Para ejemplo, todos los registros de producción y control, que incluyen registros de auditoría, deben revisarse y aprobado por la unidad de calidad. Las regulaciones brindan flexibilidad para tener algunas actividades revisadas por una persona que supervisa o verifica directamente la información.
FDA recomienda un enfoque de sistema de calidad para implementar la supervisión y revisión de cGMP registros.
¿Con qué frecuencia se deben revisar los registros de auditoría?
Si la frecuencia de revisión de los datos se especifica en las regulaciones de cGMP, adhiérase a esa frecuencia para la revisión de la pista de auditoría. Por ejemplo, requiere revisión después de cada paso significativo en fabricación, procesamiento, empaque o almacenamiento, y requiere la revisión de datos antes del lote liberar. En estos casos, aplicaría la misma frecuencia de revisión para la pista de auditoría.
Si la frecuencia de revisión de los datos no está especificada en las regulaciones de cGMP, debe determinar la frecuencia de revisión de la pista de auditoría utilizando el conocimiento de sus procesos y la evaluación de riesgos.
La evaluación de riesgos debe incluir la evaluación de la criticidad de los datos, los mecanismos de control e impacto en la calidad del producto. Los riesgos para los datos incluyen, entre otros, la posibilidad de que se eliminen modifique o excluyan sin autorización o sin detección.
Su enfoque para la revisión de la pista de auditoría y la frecuencia con la que la realiza deben garantizar que se cumplen los requisitos de cGMP, se implementan los controles apropiados y la confiabilidad de la revisión.
¿Puedo aumentar la trazabilidad de mis libros de Excel sin necesidad de usar VBA?
¡Si! y todo de manera virtual con el suso de nuestro complemento COM. Esto garantiza que tus datos sean trazados de manera perdurable.
En deappharma hemos desarrollado eDocuSeed una herramienta validada y especializada para el mantenimiento, gestión y trazabilidad de libros de Excel. ¡Sin duda te ayudaremos a mitigar tu riesgo! Puedes contactarnos para mejorar el proceso administrativo de tu organización a través software 100% confiable y seguro.
Referencias
- Data Integrity and Compliance With Drug CGMP Questions and Answers Guidance for Industry
- Guía para el enfoque de sistemas de calidad de la industria para las regulaciones CGMP farmacéuticas.
¡Contáctanos! y conoce de que manera te vamos a ayudar.
¡Únete a nuestra comunidad en redes!