2, May 2022
Características de un buen SRS (Software Requirements Specification) especificación de requerimientos de software
La especificación de requisitos de software (SRS) es una descripción completa del comportamiento del sistema que se va a desarrollar. Incluye un conjunto de casos de uso que describe todas las interacciones que tendrán los usuarios con el software. Los casos de uso también son conocidos como requisitos funcionales. Además de los casos de uso, la ERS también contiene requisitos no funcionales (complementarios). Los requisitos no funcionales son requisitos que imponen restricciones en el diseño o la implementación, como, por ejemplo, restricciones en el diseño o estándares de calidad.
Está dirigida tanto al cliente como al equipo de desarrollo. El lenguaje utilizado para su redacción debe ser informal, de forma que sea fácilmente comprensible para todas las partes involucradas en el desarrollo.
Las características de un buen SRS son:
- Sin ambigüedades
- Completa
- Verificable
- Coherente
- Modificable
- Trazable
- Utilizable durante la fase explotación y mantenimiento
Cada característica se aborda con mayor detalle a continuación:
Sin ambigüedad. Una SRS es inequívoca si- y solo si- cada requisito en ella tiene una única interpretación.
- Como mínimo, esto requiere que cada característica del producto final se describa utilizando un único termino.
- En los casos en los que un término utilizado en un contexto particular pueda tener múltiples significados, el termino debe incluirse en un glosario donde se especifique su significado.
Completa. Un SRS es completo si posee las siguientes cualidades:
- Inclusión de todos los requisitos significativo, ya sean relativos a la funcionalidad, el rendimiento, las limitaciones de diseño, los atributos o las interrelaciones externas.
- Definición de las respuestas de software a todas las clases realizables de datos de entrada en todas las clases realizables de situaciones. Obsérvese que es importante especificar la respuesta a los valores de entrada válidos y no validados.
- Conformidad con cualquier norma del SRS que le sea aplicable. Si una sección particular de la norma no es aplicable, el SRS debe incluir el número de sección y una explicación de porque no es aplicable.
Verificable. Un SRS es verificable si, y solo si, todos los requisitos establecidos en el son verificables. Un requisito es verificable si y solo si existe algún proceso finito y rentable con el que una persona o máquina pueda comprobar que el producto de software cumple con el requisito.
- Ejemplos de requisitos no verificables, estas son declaraciones como: a)El producto debe funcionar bien, o el producto debe tener una buena interfaz humana. Estos requisitos no pueden verificarse porque es imposible definir los términos bueno o bien. b)El programa nunca debe entrar en un bucle infinito. Este requisito no es verificable porque la comprobación de esta cualidad es teóricamente imposible.
Coherente. Un buen SRS es consistente si y solo si ningún conjunto de requisitos individuales descritos en ella entra en conflicto. Hay tres tipos de conflictos principales en un SRS:
- Dos o más requisitos pueden describir el mismo objeto del mundo real, pero utilizar termino diferentes para ese objeto. Por ejemplo, la solicitud de una entrada de usuarios por parte de un programa puede denominarse “prompt” en un requisito y “cue” en otro.
- Las características especificadas de los objetos del mundo real pueden entrar en conflicto. Por ejemplo: 1)El formato de un informe de salida puede describirse en un requisito como «tabular” pero en otro como “textual” 2) Un requisito puede establecer que todas las luces deben ser verdes mientras que otro establece que todas las luces deben ser azules. 3) Puede haber un conflicto lógico o temporal entre dos acciones específicas. Por ejemplo; a) Un requisito podría especificar que el programa sumará dos entradas y otro especificar que el programa las multiplicará. b) Un requisito puede establecer que A debe seguir a B, mientras que otros requieren que A y B ocurran simultáneamente.
Modificable. Un SRS es modificable si su estructura y estilo son tales que cualquier cambio necesario en el requisito puede realizarse de forma fácil, completa y coherente. Los cambios en un SRS generalmente requieren:
- Tener una organización coherente y fácil de usar, con un índice y referencias cruzada explicitas.
- No ser redundante; es decir, el mismo requisito no debe aparecer en otras partes en el SRS.
Trazable. Una SRS es trazable si el origen de cada uno de sus requisitos es claro y se facilita la referencia de cada requisito de la futura documentación de desarrollo o mejora. Se recomiendan dos tipos de trazabilidad:
- La trazabilidad hacia atrás (es decir, hacia etapas anteriores de desarrollo) depende de que cada requisito haga referencia explícita a su fuente en documentos anteriores.
- La trazabilidad hacia adelante (es decir, hacia todos los documentos generados por el SRS) depende que cada requisito del SRS tenga un nombre o número de referencia único.
Utilizable durante la fase de operación y mantenimiento. El SRS debe atender las necesidades de la fase de operación y mantenimiento, incluyendo la eventual sustitución del software.
- El mantenimiento suele ser realizado por personal no relacionado con el desarrollo original. Los cambios locales (correcciones) pueden aplicarse mediante un código. Si embargo, para los cambios de mayor alcance, la documentación sobre el diseño y los requisitos es esencial. Esto implica dos acciones:
- El SRS debe ser modificable
- El SRS debe contener un registro de todas las disposiciones especiales que aplican a los componentes individuales, tales como:
- Su criticidad
- Su relación con las necesidades sólo temporales.
- Su origen
- Este tipo de conocimiento se da por sentado en la organización de desarrollo, pero a menudo falta en la organización de mantenimiento. Si no se entiende la razón o el origen de una función, a menudo es imposible realizar un mantenimiento adecuado del software.
No olvides que todas nuestras soluciones son liberadas bajo un sistema de calidad robusto. En caso de ser necesario, puedes contactarnos para mejorar el proceso de laboratorio y administrativo de tu organización a través software 100% confiable y seguro. Recuerda que en deappharma contamos con una suite de herramientas que te ayudaran a mejorar tus procesos con un enfoque en integridad de datos. Somos expertos en la materia, por lo que procesos complejos no representa un reto para nosotros, debido a que tenemos en mente los aspectos relevantes de cumplimiento.
Referencias
-
FDA, Guidance for the Content of Premarket Submissions for Software Contained in Medical Devices
-
GAMP 5 Guide: Compliant GxP Computerized Systems
-
Guía del IEEE sobre especificaciones de requisitos de software ANSI/IEEE std 1984.
¡Contáctanos! y conoce de que manera te vamos a ayudar.
¡Únete a nuestra comunidad en redes!
- 0
- Por Team deappharma
5, Abr 2022
ICH Q14 desarrollo de métodos analíticos y el impacto sobre ICH Q2 validación de métodos analíticos
Uno de los procesos GxP relevantes dentro de la industria es el proceso de validación de método analíticos. La importancia esencial es su vinculación directa con el método analítico utilizado de rutina (Liberaciones, Estabilidades). Con la actualización “propuesta” por parte de ICH, en lo referente a los procesos analíticos de desarrollo y validación se busca que estos tengan una relación estrecha en el que el beneficio principal es la calidad por diseño y mantenimiento del estado validado.
Como bien sabemos, el objetivo de la validación de procedimientos analíticos es demostrar que el procedimiento es adecuado para el fin previsto. Sin perder de vista que los datos y resultados deben ser suficientemente confiables para la toma de decisiones.
Un estudio de validación está diseñado para proporcionar pruebas suficientes de que el procedimiento analítico cumple sus objetivos. Estos objetivos se describen con un conjunto adecuado de características de rendimiento correspondientes, que pueden variar en función de uso previsto del procedimiento analítico y la tecnología especifica seleccionada.
Con la reciente propuesta de la guía ICHQ14 se busca incluir, describir y robustecer el proceso de laboratorio por la estrecha relación que existe entre el desarrollo de métodos y la validación de estos. Con esto podremos visualizar términos como son: estrategia de validación y control, ciclo de vida y mantenimiento como parte esencial de esta. Sin perder de vista la inclusión de metodologías existentes, tales cuales no eran claramente abordadas.
La propuesta ICH Q14 atribuye que dicho proceso y los conocimientos arrojados por este, se controlen de tal manera que se pueda obtener la información sobre la finalidad prevista del procedimiento analítico, y el rendimiento de las características y criterios asociados que deben ser validados.
La siguiente figura muestra cómo se puede generar el conocimiento durante el desarrollo de un procedimiento analítico propuesto en la ICHQ14 y con esto ayudar al diseño de un estudio de validación.
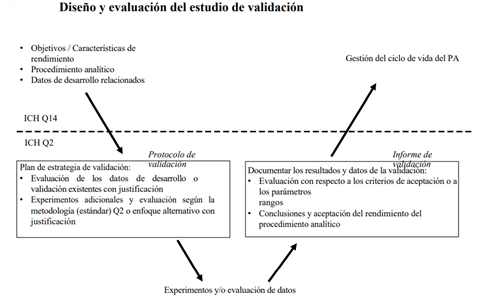
Validación durante el ciclo de vida de un procedimiento analítico
Durante el ciclo de vida de un procedimiento analítico pueden ser necesarios cambios. En tales casos, los cambios parciales pueden necesitar una revalidación completa. La ciencia y los principios basados en el riesgo pueden utilizarse para justificar sin una determinada característica de rendimiento necesita o no revalidación. El alcance de la revalidación depende de las características de rendimiento analítico afectadas por el cambio.
Consideraciones generales para el desarrollo de procedimientos analíticos y la gestión del ciclo de vida
El objetivo del desarrollo es obtener un procedimiento analítico adecuado para su propósito: medir un atributo o atributos del material analizado con la especificidad/selectividad, exactitud y/o precisión en el intervalo notificable. En esta sección se describen los enfoques mínimo y mejorado del desarrollo de procedimientos analíticos En esta sección se describen los enfoques mínimo y mejorado para el desarrollo de procedimientos analíticos. Aunque el enfoque mínimo sigue siendo aceptable, algunos o todos los elementos del enfoque mejorado de este enfoque mejorado para apoyar el desarrollo y la gestión del ciclo de vida de los procedimientos analíticos.
En ciertos casos, un procedimiento analítico establecido puede aplicarse a múltiples productos con poca o ninguna modificación de las condiciones de medición. Para una nueva aplicación de dichos procedimientos analíticos de plataforma plataforma, el desarrollo posterior puede abreviarse y algunas pruebas de validación puede omitirse sobre la base de una justificación científica y de riesgo. Los detalles de las características de rendimiento consideradas para la validación de procedimientos analíticos se describen en la ICH Q2.
En general, los datos obtenidos durante los estudios de desarrollo (por ejemplo, los datos de robustez de un diseño de de experimentos (estudio DoE)) pueden utilizarse como datos de validación para las características de rendimiento del procedimiento analítico características de rendimiento del procedimiento analítico y no es necesario repetirlos.
Enfoques mínimos frente a enfoques mejorados para el desarrollo de procedimientos analíticos
Enfoque mínimo.
El desarrollo de procedimientos analíticos debe incluir los siguientes elementos, según corresponda:
- Identificación de los atributos de la sustancia o el producto farmacéutico que deben ser analizados por el procedimiento analítico.
- Selección de una tecnología de procedimiento analítico apropiada y de los instrumentos o aparatos adecuados.
- Llevar a cabo estudios de desarrollo apropiados para evaluar el rendimiento del procedimiento analítico
- características de rendimiento del procedimiento analítico, como la especificidad, la exactitud y la precisión en el intervalo notificable (incluyendo el modelo de calibración, los límites en los extremos del rango inferior y/o superior) y la solidez.
- Definir una descripción adecuada del procedimiento analítico que incluya la estrategia de control estrategia de control del procedimiento analítico (por ejemplo, ajustes de los parámetros y adecuación del sistema).
Enfoque mejorado
El enfoque mejorado ofrece una forma sistemática de desarrollar y perfeccionar el conocimiento de un procedimiento analítico. Un enfoque mejorado debe incluir uno o más de los siguientes elementos, además de los ya descritos para el enfoque mínimo:
- Una evaluación de las propiedades de la muestra y de la variabilidad esperada de la muestra basada en conocimiento del proceso de fabricación.
- Definición del perfil analítico objetivo.
- Realización de una evaluación de riesgos y evaluación de los conocimientos previos para identificar los parámetros del procedimiento analítico que pueden afectar al rendimiento del procedimiento.
- Realización de experimentos uni o multivariados para explorar los rangos y las interacciones entre parámetros identificados del procedimiento analítico.
- Definir una estrategia de control del procedimiento analítico basada en una mejor comprensión del procedimiento incluyendo los puntos de ajuste y/o rangos apropiados para los parámetros relevantes del procedimiento analítico garantizando el cumplimiento de los criterios de rendimiento.
Definir un plan de gestión de cambios del ciclo de vida con definiciones claras y categorías de información de condiciones establecidas, rangos aceptables probados o regiones de diseño operacional del método según proceda. La aplicación de elementos del enfoque mejorado al desarrollo puede conducir a procedimientos analíticos más sólidos, a una mejor comprensión del impacto de los parámetros del procedimiento analítico y a una mayor flexibilidad para la gestión del ciclo de vida, como rangos operativos más amplios, un conjunto más apropiado de condiciones establecidas y categorías de información asociadas para los cambios.
El enfoque mejorado ofrece potencialmente varias ventajas, entre ellas
- Comprensión de aquellos atributos del procedimiento analítico tales cuales son esenciales para el rendimiento del procedimiento.
- Mejorar el control de los procedimientos analíticos para conseguir un funcionamiento más fiable.
- Permitir medidas preventivas y facilitar la mejora continua mediante el uso de más conocimiento de los procedimientos analíticos.
- Reducir la cantidad de esfuerzo a lo largo del ciclo de vida del procedimiento analítico.
El ciclo de vida del procedimiento analítico
La siguiente figura muestra los elementos del ciclo de vida del procedimiento analítico.
El desarrollo de procedimientos analíticos y los enfoques de gestión de cambios se describen en esta directriz, mientras que la validación de los procedimientos analíticos se describe en la ICH Q2. Dependiendo del uso previsto del procedimiento analítico y del enfoque de desarrollo adoptado, el orden y el alcance de cada elemento pueden variar, y varios elementos pueden darse simultáneamente.

Estrategia de control del procedimiento analítico
Una estrategia de control de procedimientos analíticos debe garantizar que el procedimiento analítico funcione como esperado durante su uso rutinario a lo largo de su ciclo de vida y consiste en un conjunto de controles, derivados de la comprensión actual del procedimiento analítico, incluidos los datos de desarrollo, la evaluación de riesgos y la robustez. El conocimiento previo también podría utilizarse para desarrollar la estrategia de control del procedimiento analítico.
La estrategia de control del procedimiento analítico debe definirse antes de la validación (ICH Q2) y debe confirmarse una vez finalizada la validación.
La estrategia de control del procedimiento analítico incluye los parámetros del procedimiento analítico que necesitan control y la prueba de idoneidad del sistema que forma parte de la descripción del procedimiento analítico. La descripción del procedimiento analítico debe incluir los pasos necesarios para realizar cada prueba analítica. Esto puede incluir (pero no se limita a) la muestra, los materiales de referencia y los reactivos, la preparación de la muestra y de control, el uso del aparato, la generación de la curva de calibración, el uso de las fórmulas con herramientas para el cálculo de los resultados notificables y otros pasos necesarios. El nivel de detalle debe permitir a un analista experto realizar el análisis e interpretar los resultados (como el nivel de detalle en una farmacopea regional para una sustancia similar). Esto se denomina comúnmente comprobación de la calidad de los datos. Se recomienda un seguimiento continuo de los resultados de los procedimientos analíticos seleccionados para buscar cualquier tendencia, de acuerdo con las expectativas. La revisión de los resultados de los procedimientos analíticos facilita la gestión del ciclo de vida del procedimiento y permite una intervención proactiva para evitar fallos.
El desafío en la revisión y mantenimiento del estado validado
La directriz ICH 14 establece de manera concisa la relación que existe entre el desarrollo de métodos, el proceso de validación y el mantenimiento del ciclo de vida con un enfoque en Calidad. Sin embargo, uno de los desafíos que enfrentamos en el día a día y llegado el momento es aquella que relaciona la obtención, disponibilidad y compilación de la información para realizar la revisión de estado validado. Sin duda la estructuración de herramientas informáticas que ayuden a mostrar y recuperar la información contenida un solo punto será de gran ayuda para dar cumplimiento a un proceso que requiere una comprensión absoluta del comportamiento y desempeño de un método analíticos durante todo su ciclo de vida.
Los alcances tecnológicos manifiestan avances de gestión que favorecen la mejora continua y el desempeño de las actividades de laboratorio.
La gestión y mantenimiento desde una perspectiva tecnológica se precisa de la siguiente manera:
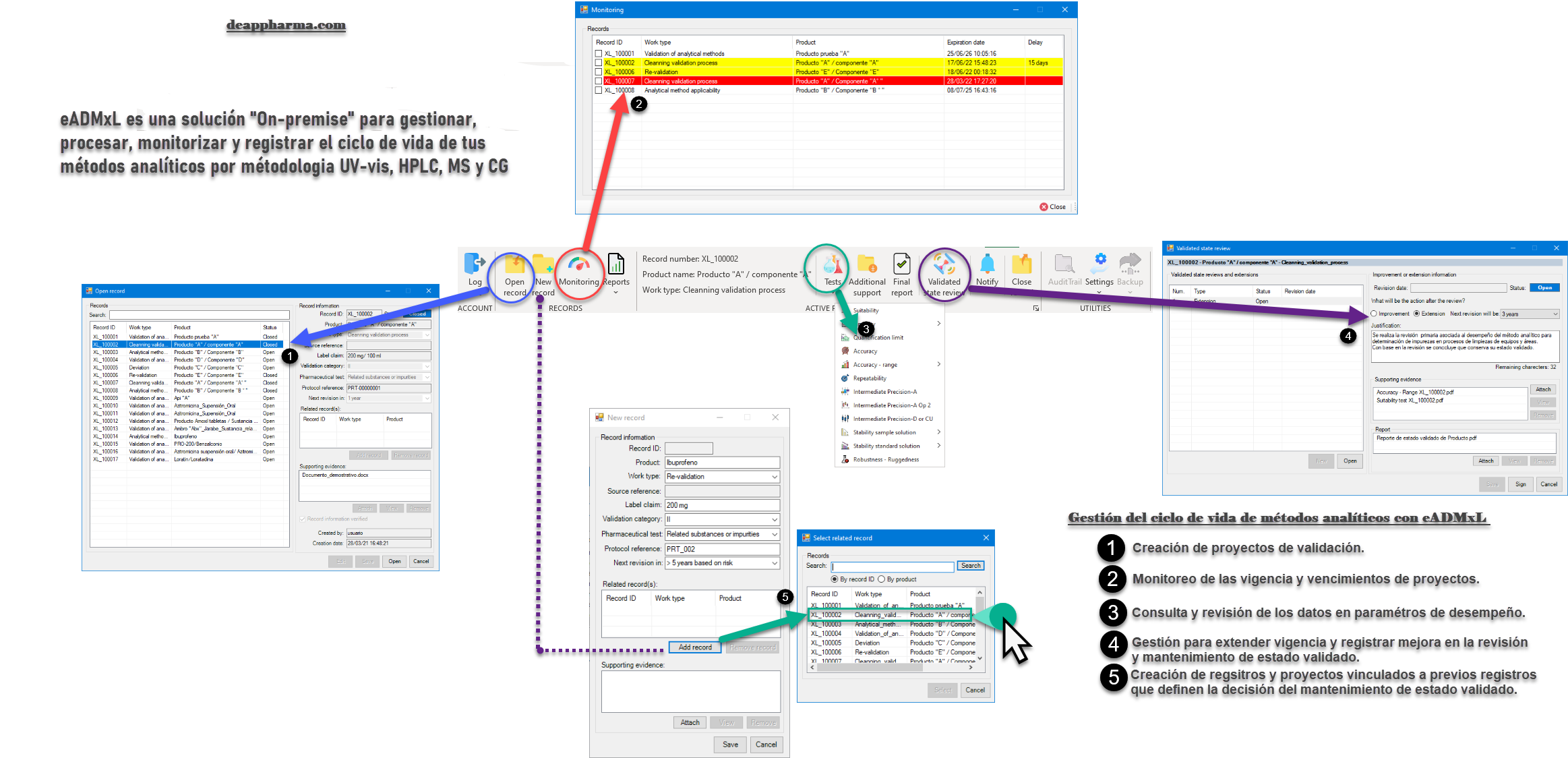
No olvides que, en caso de ser necesario, puedes contactarnos para mejorar el proceso de laboratorio y administrativo de tu organización a través software 100% confiable y seguro. Recuerda que en deappharma contamos con un software que te ayudara a controlar tu proceso de validación de métodos analíticos. Somos expertos en la materia, por lo que procesos complejos no representa un reto para nosotros, debido a que tenemos en mente los aspectos relevantes de cumplimiento.
Referencias
-
Analytical procedure development Q14 Draft version Endorsed on 24 March 2022
-
Validation of analytical procedures Q2(R2) Draft version Endorsed on 24 March 2022
¡Contáctanos! y conoce de que manera te vamos a ayudar.
¡Únete a nuestra comunidad en redes!
25, Feb 2022
¿Qué es un backup?
Entonces, definiremos como al backup, también llamado copia de respaldo o de seguridad, como la copia de la información sensible de un sistema informático desde su medio o medios de almacenamiento a un medio distinto de éste, sea cual fuere esta información, para su posterior almacenamiento en un entorno seguro con el supuesto fin de recuperar esta información con la mayor confiabilidad posible, si fuera necesario, en caso de que cualquier motivo o incidente genere la pérdida o modificación no deseada de los datos originales, para de esta manera obtener nuevamente, en un tiempo conveniente y razonable, la operatividad (consecuencia directa de la información) del sistema de cual se hizo la copia previa al incidente.
Cuando mencionamos que al realizar un backup copiamos la información sensible, nos referimos a los datos y metadatos que conforman el sistema informático. Es decir, que al realizar la copia de de la información con el objetivo de respaldarla no basta con copiar archivos, directorios o bases de datos, sino que los copiaremos con todas la características y cualidades, es decir, no sólo se trata de resguardar la información contenida en el archivo. Es importante mantener la estructura o imagen de estos al momento de realizar el backup, es decir, su ubicación (path), privilegios o permisos, si son de lectura, de sistema, etc.
Por otro lado, también mencionaremos el destino de esta copia, la cual debe hacerse a un medio distinto y en un entorno seguro. No nos serviría de nada generar una copia de la información en el mismo disco en el cual estamos trabajando o mantener el soporte destino junto al equipo. En ambos casos tanto la información original como el respaldo comparten los mismos riesgos, y esto es, precisamente lo que deseamos evitar.
Así mismo, el proceso se realiza presuponiendo cierta confiabilidad, pero no toda. En primer lugar, porque tampoco estamos exentos de que el soporte destino falle, éstos corren los mismos riesgos que los medios de origen, aunque en menor medida. En segundo lugar, porque puede existir un intervalo de tiempo significativo entre el día y la hora los cuales se ejecutó el proceso del backup y el día la hora en los cuales deseamos recuperar la información.
Por último, cuando mencionamos recuperar la información en un tiempo conveniente y razonable, nos referimos a la severidad con la que la información debe estar disponible nuevamente. Si bien la fiabilidad del backup es proteger nuestros datos, no nos sirve de mucho si los tiempos de recuperación son excesivos.
Si bien la tarea puede considerarse incomodo, y muchas veces sin sentido, nos evitará, sin ninguna duda, situaciones que hagan peligrar la operatividad de nuestros sistemas, y el ahorro de muchas situaciones irremediables.
Junto al termino backup aparece otro no menos importante: restore (recuperación o restauración), que es la operación inversa al backup. O sea, copiar al sitio original, desde el soporte destino, la información a la cual se le realizó backup anteriormente.
En muchas oportunidades se considera erróneamente backup a la copia de la información que se realiza en el mismo disco físico que contiene la información original, o tal vez se entiende que un nivel RAID es una especie de bakup, y no lo es. Si bien esta copia puede resultar útil en caso de modificaciones no deseadas o corrupción de la información del archivo o archivos originales, no nos permite recuperar la información en el caso de que la falla provenga del disco físico y nos provea estados del sistema anteriores al actual.
Por consiguiente, cuando hablamos de backup, nos referimos, no solo a copiar, sino pa hacerlo a un medio distinto del original. La idea conceptual del backup es extraer la información del sistema informático para ponerla a salvo, es decir, almacenarla en un entorno seguro. O, al menos, en un entorno que no comparta los mismos riesgos que el medio de origen.
No olvides que en caso de ser necesario, puedes contactarnos para mejorar el proceso de laboratorio y administrativo de tu organización a través software 100% confiable y seguro. Recuerda que en deappharma somos expertos en la materia, por lo que procesos complejos no representa un reto para nosotros, debido a que tenemos en mente los aspectos relevantes de cumplimiento.
Referencias
- Administración de Storage y Backups_Dante cantone, España, Editorial Alfa Omega
¡Contáctanos! y conoce de que manera te vamos a ayudar.
¡Únete a nuestra comunidad en redes!
11, Feb 2022
Audit Trail para asegurar y elevar el proceso de Integridad de datos
Este término regulatorio e informático se refiere a la auditoría, detección continua y exhaustiva de los datos. Por lo que es relevante contar con este proceso o función en cada uno de nuestros sistemas informatizados. El objetivo, es trazar la vida de un dato de manera perdurable.
La industria farmacéutica, dispositivos médicos y almacenes utilizan sistemas informatizados dentro de sus procesos. Por este hecho, es relevante el control y trazabilidad de datos. Para abordar el tema y conocer el alcance e importancia de la función de pistas de auditoria te invitamos a leer lo siguiente.
¿Qué es un “pista de auditoría”?
La «Pista de auditoría» o también conocida como «Audit Trail». Significa un registro electrónico seguro, generado por computadora con sellos de tiempo que permiten la reconstrucción del curso de los eventos relacionados con la creación, modificación y/o eliminación de un registro electrónico. Por ejemplo, la pista de auditoría para una ejecución de cálculos analíticos con la utilización de Excel como software de cálculo, debe incluir como mínimo lo siguiente: nombre de usuario, la fecha/hora de la ejecución, los cambios realizados sobre un valor y los detalles justificados de dicho cambio, según apliquen. ¡Pero no solo eso! Las pistas de auditoria son un aparte esencial de los sistemas computarizados. Es por esto, que los reportes de auditorita deben ser robustos y seguros.
Retomemos el ejemplo de uso de la hoja de Excel para obtención de resultados analíticos. En la actualidad la industria configura la obtención de pistas de auditoría sobre los mismos libros de Excel. Esta pista «LOG» regularmente la establecen dentro del mismo libro de manera anidada como una pestaña (hoja) de cálculo. ¡Esta práctica, es poco sostenible y segura! ya que la trazabilidad la dejas en manos de Excel y de la vulnerabilidad de código realizado con VBA.
¿Existe riesgo de perder la trazabilidad en mis libros de Excel por usar configuración VBA?
La respuesta es ¡Si! y tu impacto será alto porque no tendrás la manera de trazar la información.
Los riesgos los podemos clasificar en dos escenarios posibles:
- Daño en el archivo de Excel que no permita acceder a la información.
- Alteración y vulnerabilidad de la programación en VBA (Hasta videos en youtube te enseñan a desbloquear código relizadoo con VBA. ¡Ojo con esto!)
¿Quién debe revisar los registros de auditoría?
La revisión de la pista de auditoría es similar a la evaluación de las tachaduras en papel al revisar los datos. Personal responsable de la revisión de registros bajo cGMP debe revisar las pistas de auditoría que capturan los cambios en datos asociados con el registro a medida que revisan el resto del registro. Para ejemplo, todos los registros de producción y control, que incluyen registros de auditoría, deben revisarse y aprobado por la unidad de calidad. Las regulaciones brindan flexibilidad para tener algunas actividades revisadas por una persona que supervisa o verifica directamente la información.
FDA recomienda un enfoque de sistema de calidad para implementar la supervisión y revisión de cGMP registros.
¿Con qué frecuencia se deben revisar los registros de auditoría?
Si la frecuencia de revisión de los datos se especifica en las regulaciones de cGMP, adhiérase a esa frecuencia para la revisión de la pista de auditoría. Por ejemplo, requiere revisión después de cada paso significativo en fabricación, procesamiento, empaque o almacenamiento, y requiere la revisión de datos antes del lote liberar. En estos casos, aplicaría la misma frecuencia de revisión para la pista de auditoría.
Si la frecuencia de revisión de los datos no está especificada en las regulaciones de cGMP, debe determinar la frecuencia de revisión de la pista de auditoría utilizando el conocimiento de sus procesos y la evaluación de riesgos.
La evaluación de riesgos debe incluir la evaluación de la criticidad de los datos, los mecanismos de control e impacto en la calidad del producto. Los riesgos para los datos incluyen, entre otros, la posibilidad de que se eliminen modifique o excluyan sin autorización o sin detección.
Su enfoque para la revisión de la pista de auditoría y la frecuencia con la que la realiza deben garantizar que se cumplen los requisitos de cGMP, se implementan los controles apropiados y la confiabilidad de la revisión.
¿Puedo aumentar la trazabilidad de mis libros de Excel sin necesidad de usar VBA?
¡Si! y todo de manera virtual con el suso de nuestro complemento COM. Esto garantiza que tus datos sean trazados de manera perdurable.
En deappharma hemos desarrollado eDocuSeed una herramienta validada y especializada para el mantenimiento, gestión y trazabilidad de libros de Excel. ¡Sin duda te ayudaremos a mitigar tu riesgo! Puedes contactarnos para mejorar el proceso administrativo de tu organización a través software 100% confiable y seguro.
Referencias
- Data Integrity and Compliance With Drug CGMP Questions and Answers Guidance for Industry
- Guía para el enfoque de sistemas de calidad de la industria para las regulaciones CGMP farmacéuticas.
¡Contáctanos! y conoce de que manera te vamos a ayudar.
¡Únete a nuestra comunidad en redes!
24, Ene 2022
Detalles del Enfoque – Alcance de la Parte 11 de CFR
Detalles del Enfoque – Alcance de la Parte 11
Interpretación estrecha del alcance
Entendemos que existe cierta confusión sobre el alcance de la parte 11. Algunos han entendido que el alcance de la parte 11 es muy amplio. Creemos que algunas de esas amplias interpretaciones podrían conducir a controles y costos innecesarios y podrían desalentar la innovación y los avances tecnológicos sin brindar un beneficio adicional a la salud pública. Como resultado, queremos aclarar que la Agencia tiene la intención de interpretar el alcance de la parte 11 de manera restringida.
Según la interpretación restringida del alcance de la parte 11, con respecto a los registros que deben mantenerse según las reglas predicadas o presentarse a la FDA, cuando las personas optan por utilizar registros en formato electrónico en lugar de papel, se aplicaría la parte 11. Por otro lado, cuando las personas usan computadoras para generar impresiones en papel de registros electrónicos, y esos registros en papel cumplen con todos los requisitos de las reglas predicadas aplicables y las personas confían en los registros en papel para realizar sus actividades reguladas, la FDA generalmente no condicionara a las personas para «usar registros electrónicos en lugar de registros en papel». En estos casos, el uso de sistemas informáticos en la generación de registros en papel no activaría la parte 11.

Definición de registros de la Parte 11
Bajo esta interpretación estrecha, la FDA considera que la parte 11 es aplicable a los siguientes registros o firmas en formato electrónico (registros o firmas de la parte 11):
- Registros que deben mantenerse según los requisitos de la regla establecida y que se mantienen en formato electrónico en lugar del formato en papel. Por otro lado, los registros (y cualquier firma asociada) que no se requiera conservar según las reglas establecida, pero que, sin embargo, se mantienen en formato electrónico, no son registros de la parte 11.
Le recomendamos que determine, en función de las reglas establecidas, si los registros específicos son registros de la parte 11. Le recomendamos que documente tales decisiones.
- Registros que deben mantenerse según las reglas establecidas, que se mantienen en formato electrónico además del formato en papel, y en los que se confía para realizar actividades reguladas.
En algunos casos, las prácticas comerciales reales pueden dictar si está utilizando registros electrónicos en lugar de registros en papel. Por ejemplo, si se requiere que se mantenga un registro bajo una regla predicada y usted usa una computadora para generar una copia impresa en papel de los registros electrónicos, pero aun así depende del registro electrónico para realizar actividades reguladas, la Agencia puede considerar que usted está utilizando el registro electrónico en lugar del registro en papel. Es decir, la Agencia puede tener en cuenta sus prácticas comerciales para determinar si se aplica la parte 11.
En consecuencia, recomendamos que, para cada registro que deba mantenerse según las reglas establecidas, determine de antemano si planea confiar en el registro electrónico o en el registro en papel para realizar actividades reguladas. Recomendamos que documente esta decisión (por ejemplo, en un Procedimiento operativo estándar (SOP) o documento de especificación).
Registros enviados a la FDA, conforme a reglas establecidas (incluso si dichos registros no están específicamente identificados en las reglamentaciones de la Agencia) en formato electrónico. Sin embargo, un registro que no se presenta en sí mismo, pero que se utiliza para generar una presentación, no es un registro de la Parte 11 a menos que se requiera que se mantenga bajo una regla establecida y se mantenga en formato electrónico.
Firmas electrónicas que pretenden ser el equivalente de firmas manuscritas, iniciales y otras firmas generales requeridas por reglas establecidas. Las firmas de la Parte 11 incluyen firmas electrónicas que se utilizan, por ejemplo, para documentar el hecho de que ciertos eventos o acciones ocurrieron de acuerdo con la regla establecida (por ejemplo, aprobado, revisado y verificado).
Enfoque de los requisitos específicos de la Parte 11
Validación
La Agencia tiene la intención de ejercer la discreción de cumplimiento con respecto a los requisitos específicos de la parte 11 para la validación de sistemas computarizados y los requisitos correspondientes. Aunque las personas aún deben cumplir con todos los requisitos de las reglas establecidas aplicables para la validación, esta guía no debe interpretarse como una imposición de requisitos adicionales para la validación.
Sugerimos que su decisión de validar los sistemas computarizados y el alcance de la validación tengan en cuenta el impacto que los sistemas tienen en su capacidad para cumplir con los requisitos de las reglas establecidas. También debe considerar el impacto que esos sistemas podrían tener en la precisión, confiabilidad, integridad, disponibilidad y autenticidad de los registros y firmas requeridos. Incluso si no existe un requisito de regla de establecido para validar un sistema, en algunos casos puede ser importante validar el sistema.
Recomendamos que base su enfoque en una evaluación de riesgos justificada y documentada y una determinación del potencial del sistema para afectar la calidad y seguridad del producto y la integridad del registro. Por ejemplo, la validación no sería importante para un procesador de texto que se usa solo para generar SOP.
Pista de auditoría
La Agencia tiene la intención de ejercer la discreción de cumplimiento con respecto a los requisitos específicos de la parte 11 relacionados con las pistas de auditoría generadas por computadora y con sello de tiempo y cualquier requisito correspondiente. Las personas aún deben cumplir con todos los requisitos de reglas establecidas aplicables relacionados con la documentación de, por ejemplo, fecha, hora o secuencia de eventos, así como cualquier requisito para garantizar que los cambios en los registros no oscurezcan entradas previas.
Incluso si no existen requisitos de reglas establecidas para documentar, por ejemplo, la fecha, la hora o la secuencia de eventos en una instancia particular, puede ser importante contar con pistas de auditoría u otras medidas de seguridad físicas, lógicas o de procedimiento para garantizar la confiabilidad y confiabilidad de los registros. Le recomendamos que base su decisión de aplicar pistas de auditoría u otras medidas apropiadas, en la necesidad de cumplir con los requisitos de la regla establecida, una evaluación de riesgos justificada y documentada, y una determinación del efecto potencial sobre la calidad y seguridad del producto y la integridad del registro. Le sugerimos que aplique los controles apropiados basados en dicha evaluación. Los registros de auditoría pueden ser particularmente apropiados cuando se espera que los usuarios creen, modifiquen o eliminen registros regulados durante el funcionamiento normal.
Sistemas heredados
La Agencia tiene la intención de ejercer la discreción de ejecución con respecto a todos los requisitos de la parte 11 para los sistemas que de otro modo estaban operativos antes del 20 de agosto de 1997, la fecha de vigencia de la parte 11, bajo las circunstancias especificadas a continuación.
Esto significa que la Agencia no tiene la intención de tomar medidas de cumplimiento para imponer el cumplimiento de los requisitos de la parte 11 si se cumplen todos los siguientes criterios para un sistema específico:
- El sistema estaba operativo antes de la fecha de vigencia.
- El sistema cumplió con todos los requisitos de reglas establecidas aplicables antes de la fecha de vigencia.
- Actualmente, el sistema cumple con todos los requisitos de reglas establecidas aplicables.
- Tiene evidencia documentada y justificación de que el sistema es apto para el uso previsto (lo que incluye tener un nivel aceptable de seguridad e integridad de registros, si corresponde).
Si un sistema ha cambiado desde el 20 de agosto de 1997, y si los cambios impiden que el sistema cumpla con los requisitos de la regla establecidad, los controles de la Parte 11 deben aplicarse a los registros y firmas de la Parte 11 de conformidad con la política de cumplimiento expresada en esta guía.
Copias de Registros
La Agencia tiene la intención de ejercer la discreción de ejecución con respecto a los requisitos específicos de la parte 11 para generar copias de registros y cualquier requisito correspondiente. Debe proporcionar a un investigador un acceso razonable y útil a los registros durante una inspección. Todos los registros en su poder están sujetos a inspección de acuerdo con las reglas establecidas.
Recomendamos que proporcione copias de registros electrónicos por:
- Producir copias de registros mantenidos en formatos portátiles comunes cuando los registros se mantienen en estos formatos
- Usar métodos de conversión o exportación automatizados establecidos, cuando estén disponibles, para hacer copias en un formato más común (los ejemplos de dichos formatos incluyen, entre otros, PDF, XML o SGML)
En cada caso, recomendamos que el proceso de copiado produzca copias que conserven el contenido y el significado del registro. Si tiene la capacidad de buscar, ordenar o buscar tendencias en los registros de la parte 11, las copias entregadas a la Agencia deben proporcionar la misma capacidad si es razonable y técnicamente factible. Debe permitir la inspección, revisión y copia de registros en un formato legible en su sitio utilizando su hardware y siguiendo sus procedimientos y técnicas establecidos para acceder a los registros.
Retención de registros
La Agencia tiene la intención de ejercer la discreción de ejecución con respecto a los requisitos de la parte 11 para la protección de registros para permitir su recuperación precisa y rápida durante todo el período de retención de registros y cualquier requisito correspondiente. Las personas aún deben cumplir con todos los requisitos de reglas establecidas aplicables para la retención y disponibilidad de registros.
Sugerimos que su decisión sobre cómo mantener los registros se base en los requisitos de las reglas predicadas y que base su decisión en una evaluación de riesgos justificada y documentada y en una determinación del valor de los registros a lo largo del tiempo.
FDA no tiene la intención de objetar si usted decide archivar los registros requeridos en formato electrónico en medios no electrónicos como microfilm, microficha y papel, o en un formato de archivo electrónico estándar (ejemplos de tales formatos incluyen, entre otros, PDF, XML o SGML). Las personas aún deben cumplir con todos los requisitos de las reglas establecidas, y los propios registros y cualquier copia de los registros requeridos deben conservar su contenido y significado. Siempre que los requisitos de la regla establecida se cumplan por completo y el contenido y el significado de los registros se conserven y archiven, puede eliminar la versión electrónica de los registros. Además, los componentes de firmas y registros en papel y electrónicos pueden coexistir (es decir, una situación híbrida) siempre que se cumplan los requisitos de la regla establecida y se conserve el contenido y el significado de esos registros.
No olvides que en caso de ser necesario, puedes contactarnos para mejorar el proceso de laboratorio y administrativo de tu organización a través software 100% confiable y seguro. Recuerda que en deappharma somos expertos en la materia, por lo que procesos complejos no representa un reto para nosotros, debido a que tenemos en mente los aspectos relevantes de cumplimiento.
REFERENCES
- Glossary of Computerized System and Software Development Terminology (Division of Field Investigations, Office of Regional Operations, Office of Regulatory Affairs, FDA 1995)
- General Principles of Software Validation; Final Guidance for Industry and FDA Staff (FDA, Center for Devices and Radiological Health, Center for Biologics Evaluation and Research, 2002)
- Guidance for Industry, FDA Reviewers, and Compliance on Off-The-Shelf Software Use in Medical Devices (FDA, Center for Devices and Radiological Health, 1999)
- Pharmaceutical CGMPs for the 21st Century: A Risk-Based Approach; A Science and Risk-Based Approach to Product Quality Regulation Incorporating an Integrated Quality Systems ApproachExternal Link Disclaimer (FDA 2002)
¡Contáctanos! y conoce de que manera te vamos a ayudar.
¡Únete a nuestra comunidad en redes!
12, Ene 2022
Ciclo de vida de la información
En la actualidad las instituciones y empresas producen, almacenan y respaldan gran cantidad e información. Hoy en día, la información que posee una empresa es uno de sus valores mas importantes. Este valor no solo es mantener un acceso rápido a los dispositivos que la almacenan. Existen casos donde no se justifica el gasto porque el valor de la información no siempre es el mismo. El veloz crecimiento del volumen de información no puede ser excusa para no organizar esta información según su criticidad y volumen. Cuando la información de una empresa o institución no se encuentra ordenada y clasificada se producen inconvenientes que dificultan su procesamiento ya que se presentan diferentes tiempos de acceso a la información.
El concepto de ciclo de vida esta evolucionado rápidamente en la industria de la información (medianas y grandes empresas) junto al valor que le otorga la información. La idea que sustenta el ciclo de vida es el concepto de la cadena de valor que posee una información en particular desde que se crea hasta que se accede a ella en mayor o menor medida. En estos accesos pasa por una serie de procesos cuya función es añadir valor para quien debe utilizarla hasta agotar su funcionalidad. Sucede que al aumentar el valor de la información también se aumenta el coste de almacenamiento.
Los inconvenientes mencionados surgen ya que el desorden o falta de clasificación se produce por no acceder a la información por los mismos canales o bajo las mismas pautas y los detallamos a continuación.
1.1-Dificultad de acceder a llegar a la información
Mencionábamos que una organización depende de la información que tiene almacenada para poder llevar a cabo sus objetivos. Que el volumen de información esté informatizado no implica que esté de forma ordenada, es decir, que los integrantes de la información sepan cómo, o tengan los medios necesarios para acceder a la información. Éste es el primer obstáculo a superar cuando hablamos de gestionar información dentro del ciclo de vida.
1.2.-Deficiencia en el acceso en cuanto a tiempo y forma
Superado el primer inconveniente, nuestra tarea continua en mejorar el acceso a la información considerando los aspectos técnicos. En esta tarea lo principal es el análisis de los requerimientos de la organización y del relevamiento del hardware disponible para llevar adelante las operaciones.
1.3.-Diferentes modos de acceder a la información
Por último, pondremos foco en mejorar el acceso a la información teniendo presente los aspectos externos al hardware y dependientes de cada uno de los usuarios o áreas que necesitan acceder.
Muchas veces para mitigar o corregir parcialmente estos inconvenientes se intenta alojar la mayor cantidad de información en servidores con discos duros (de alto rendimiento). Ya que el alojamiento en estos servidores ayudan a mantener, gestionar, hacer peticiones y establecer conexiones de bases de datos que ayudan con el orden de información.
Ya hemos dicho que el significado y la importancia de esta información serán los mismos a medida que transcurre el tiempo. Debido a esto la forma, los métodos y las técnicas con que debe ser almacenada y respaldada la información cambiaran de acuerdo al paso del tiempo, ya que la información no tendrá el mismo valor, es decir, el concepto principal que obtenemos del ciclo de vida de la información es almacenar la información donde podremos obtener el mejor beneficio de ella.
Relevar y analizar los puntos antes mencionados nos proporcionaran una idea muy acertada de cómo encarar al almacenamiento y, si fuera necesario, protección (backups) de la información concerniente al sistema que estamos analizando, diseñado o administrando.
No olvides que en caso de ser necesario, puedes contactarnos para mejorar el proceso de laboratorio y administrativo de tu organización a través software 100% confiable y seguro. Recuerda que en deappharma somos expertos en la materia, por lo que procesos complejos no representa un reto para nosotros, debido a que tenemos en mente los aspectos relevantes de cumplimiento.
Referencia;
- Administración de Storage y Backups_Dante cantone, España, Editorial Alfa Omega
¡Contáctanos! y conoce de que manera te vamos a ayudar.
¡Únete a nuestra comunidad en redes!
20, Dic 2021
Hojas de cálculo con integridad de datos con cumplimiento CFR21
Las industrias reguladas utilizan las hojas de cálculo para muchos propósitos. Haciendo que Excel cubra diferentes necesidades atribuidas a las actividades de rutina. Este programa «Excel» puede: calcular, organizar y analizar datos, de tal manera que pueda evaluar el funcionamiento de: procesos, métodos, tendencias y en algunas ocasiones la obtención de documentos, con base en plantillas que se alimentan de bases de datos creadas propiamente en la misma aplicación. Las hojas de cálculo se configuran en un formato de cuadrícula. Cada pieza de información se coloca en su propia celda para que pueda ser usada adecuadamente. Los datos pueden ser números o palabras. Las palabras se organizan alfabéticamente y los números numéricamente. Los números se calculan con suma, resta, multiplicación, división y en algunos casos estadística más avanzada. Partiendo de esto , el uso de hojas de cálculo dentro de la industria regulada toma relevancia, ya que impacta en mayor medida sobre procesos de carácter GxP.
La situación actual
La versatilidad de las hojas de cálculo proporciona opciones de diferentes alcances GxP, por ejemplo;
Bases de datos, con el siguiente alcance:
- Control de muestras
- Control de resultados de resultados de laboratorio
- Listado de muestreos de materiales
- Listado de muestra de retención
- Listado de estatus de documento
- Asignación de código de documentos
- Listados maestros de estabilidades
- Listados de toma de muestras para programa anual, entre otros.
Hojas de cálculo, con el siguiente alcance:
- Emisión de resultados de: ensayo, uniformidad de contenido, sustancias relacionadas, disolución
- Evaluación de todos parámetros de desempeño del proceso de validación de métodos analíticos
- Evaluación de resultados de perfiles de disolución, entre otros.
Plantillas, con el siguiente alcance:
- Emisión de certificados de análisis
- Emisión de protocolos
- Emisión de reportes, entre otros.
Derivado del dinamismo y la versatilidad de la aplicación Excel, podemos obtener diferentes magnitudes de hallazgos relacionadas a eventos de integridad de datos, tales cuales ponen en cuestionamiento el cumplimiento regulatorio.
Las situaciones relevantes por el uso de hojas de cálculo son los siguientes:
Desarrollo
- Desarrollo de plantillas con esquemas de reedición
- Desarrollo de plantillas en los que no ha sido retada la estadística contenida en estas
- Desarrollo de fórmulas estadísticas establecidas, sin una base de conocimiento estadístico.
Funcionalidad
- No cuentan con perfiles robustos para el ingreso a la plantilla, niveles de usuario y definición del alcance de estos para el desempeño en el uso de mismas
- No hay validación de las celdas, discriminando si son numéricas o textuales
- Seguridad de las hojas solo estableciendo contraseñas con las propiedades de Excel o con métodos poco robustos como VBA (Visual Basic Application)
- No se puede justificar y atribuir a alguien el cambio y/o modificación de un dato-valor
- La seguridad de la hoja se da con el bloqueo de la misma
- Se pueden copiar y pegar las hojas en otras rutas
- Uso de hojas multiusuario.
Integridad de datos
- No cuentan con Audit trail “pistas de auditoria” (elemento crítico para dar trazabilidad a cada movimiento realizado en un entorno GxP computarizado)
- No cuentan con la capacidad de respaldo y recuperación de la información
- Los datos no se asocian con bases de datos que hagan que estos perduren y, por tanto no pueden ser mantenidos; Atribuibles,legibles, contemporáneos y exactos (ALCOA).
Principio
Derivado de los puntos y controles sugeridos por las agencias regulatorias con el fin de garantizar la integridad de datos y con esto mantener el concepto de “ALCOA ++” partiendo de que los datos sean perdurables, se necesitan infraestructuras para garantizar la misma.
ALCOA ++, se atribuye a los siguientes términos:
- Atribuible, todas las actividades tales como crear, borrar o modificar son relacionadas a un individuo.
- Legible, la información debe ser clara y visible.
- Contemporáneo, la información debe ser registrada en el momento de hacer la actividad.
- Original, los datos deben provenir de registros originales o copias fieles a la original.
- Exactos, la exactitud debe ser controlada para eliminar errores y los cambios deben ser documentados.
- +Completo, todos los datos pertenecientes al registro GxP deberán ser retenidos.
- +Consistente, la línea del tiempo del metadato debe ser lógico.
- +Duradero, todos los registros deben estar en un medio duradero de manera legible durante su tiempo de retención.
- +Disponible, los datos deberán estar disponibles y accesibles en su totalidad.
Qué refiere una hoja de cálculo con integridad?
Las hojas de cálculo con integridad de datos, manifiestan un alto comportamiento en la trazabilidad y vida de un dato-valor, de tal manera que la perdurabilidad de este sea consistente y por tanto se pueda mantener: atribuible, legible, contemporáneo y exacto.
Suponga que está utilizando una hoja de cálculo y que necesita cambiar los valores obtenidos de al menos una prueba dentro de una fila. Tiene un pequeño problema: tiene que cambiar el valor de varias filas. Por ejemplo, el pH aparece en tres filas. Pero aparecerá un problema de verdad si olvida cambiar uno de los valores de las filas – el valor de pH asignado a esta fila se volverá ambigua, y por tanto sus datos perderán integridad.
Como hacer que una hoja de cálculo tenga Integridad de datos?
Las hojas de cálculo se deben evaluar y, con base en esto determinar el alcance GxP.

Derivado de la determinación, podemos considerar el diseño del sistema computarizado. Para esta transformación se necesitan procesos de programación mediante lenguajes robustos obtenidos por aplicaciones. Las hojas de cálculo más recientes con enfoque a entornos y control de datos GxP tiene estas capacidades.
CFR21 parte 11.10 «Controles»
Cuando hacemos referencias a hojas de cálculo, estas deben ser tratadas como un sistema computarizado. Por este hecho a esta herramienta le aplican los siguientes controles regulatorios y de cumplimiento:
- Debe permitir el proceso de validación para garantizar la precisión, la confiabilidad, el desempeño esperado consistente y la capacidad de discernir registros inválidos o alterados.
- Debe proporcionar la capacidad de generar copias precisas y completas de los registros en forma legible y en formato electrónico, para que la entidad reguladora pueda inspeccionarlos, revisarlos y copiarlos.
- Debe permitir la recuperación precisa , durante todo el período de retención de registros.
- Debe limitar el acceso del sistema a personas autorizadas.
- Debe usar pistas de auditoría seguras, generadas por computadora y con marca de tiempo, para registrar de manera independiente la fecha y la hora de las entradas y acciones del operador que crean, modifican o eliminan registros electrónicos. Los cambios de registro no deben ocultar la información previamente grabada.
- Debe permitir establecer el cumplimiento de políticas escritas, que responsabilizan a las personas de las acciones iniciadas bajo sus firmas electrónicas, con el fin de impedir la falsificación de registros y firmas.
- Debe proporcionar controles de autoridad, para garantizar que solo las personas autorizadas puedan usar el sistema, firmar electrónicamente un registro, acceder a la operación o al dispositivo de entrada o salida del sistema informático, alterar un registro o realizar operación en cuestión.
- Debe tener controles adecuados sobre la distribución, el acceso y el uso de la documentación para la garantizar su trazabilidad.
Por qué es importante la integridad de datos?
La importancia radica en disminuir el riesgo de que los datos críticos pueden ser falseados, borrados, divulgados sin autorización, modificados o negados por los emisores. Y con esto, no tener la posibilidad de trazar la historia y/o auditarla.
Lineamientos regulatorios a considerar
Todos los registros de calidad y técnico/científicos (incluyendo informes de análisis, certificados de análisis y hojas de trabajo analítico) deben ser legibles, rápidamente recuperables, almacenados y retenidos dentro de instalaciones que proporcionen un medio ambiente adecuado que prevenga modificaciones, daño o deterioro y/o pérdida.
Las condiciones bajo las cuales todos los registros originales son almacenados deben ser tales que aseguren su seguridad y confidencialidad, y el acceso a ellos debe estar restringido al personal autorizado. Se pueden emplear también almacenamiento y firmas electrónicos, pero con acceso restringido y en conformidad con los requisitos de los registros electrónicos.
Disposiciones asociadas a sistemas cerrados (incluye hojas de Excel)
- Limitar el acceso al sistema a personas autorizadas.
- Uso de verificaciones del sistema operativo.
- Uso de controles de autoridad.
- Determinación de que las persona que desarrollan , mantienen o usas sistemas tienen la educación , capacitación y experiencia para realizar las tareas asignadas.
- Establecimiento de políticas escritas que responsabilizan a las personas por las acciones iniciadas bajo sus firmas electrónicas.
- Controles apropiados sobre la documentación de los sistemas.
No olvides que en caso de ser necesario, puedes contactarnos para mejorar el proceso de laboratorio y administrativo de tu organización a través software 100% confiable y seguro. Recuerda que en deappharma somos expertos en la materia, por lo que procesos complejos no representa un reto para nosotros, debido a que tenemos en mente los aspectos relevantes de cumplimiento. ¡Conoce nuestras soluciones da clic aquí!
Referencias
- CFR 21 Parte 11.10 Closed systems
- FDA Data Integrity and Compliance With CGMP Guidance for Industry
- NOM 059 2015 Buenas prácticas de fabricación de medicamentos.
- WHO Technical Report Series, No. 957, 2010 44th Report – Annex 1 Buenas prácticas de la OMS para laboratorios de control de calidad de productos farmacéuticos
¡Contáctanos! y conoce de que manera te vamos a ayudar.
¡Únete a nuestra comunidad en redes!
2, Dic 2021
Buenas prácticas de documentación digital.
A partir del desarrollo de las tecnologías de la información se han descubierto campos inéditos como el de la documentación en soporte digital que, sin duda, a planteado nuevos retos en torno a su administración, acceso y preservación. De hecho, a causa del aumento de documentos en soporte digital, tanto la archivística como la tecnología han visto la necesidad de desarrollar políticas, estrategias y actividades tendientes a enfrentar este nuevo desafío, el cual, reclama acciones inmediatas y en la medida de lo posible soluciones estandarizadas a nivel internacional.
Qué es un documento digital?
Desde una perspectiva terminológica, sostiene que, el documento digital son datos o información que han sido capturados y fijados para su almacenamiento y manipulación en un sistema automatizado y que requieren del uso de este para hacerlo accesible a una persona. Se puede decir entonces que, este tipo de documentos son producidos a través de procesadores de texto, hojas de cálculo y gráficos que constituyen los resultados de distintos programas o paquetes de software. De allí la importancia de estos programas para la visualización de los documentos digitales debido a que actúan como un intermediario entre el hardware y la persona que está accediendo a la información
Una perspectiva diferente la proporciona el Modelo de Requisitos para la Gestión de Documentos Electrónicos de Archivo , que lo define como un documento que está en forma electrónica/digital porque ha sido creado mediante un programa informático o bien porque se ha digitalizado por ejemplo, cuando se ha escaneado a partir de un documento en papel. Asimismo, se puede puntualizar como un documento analógico o digital que es transportado por un conducto eléctrico y requiere del uso de equipamiento para ser inteligible por parte de una persona. En consecuencia y comparando las anteriores concepciones sobre el documento digital, coinciden en que se trata de información que se encuentra en soporte digital, que además posee un conjunto de códigos que precisan de una herramienta de tipo eléctrico para ser decodificado con el fin de hacerlo accesible al usuario. Son entonces, documentos que han sido creados en un entorno digital y que para su reproducción y accesibilidad requieren de un hardware (partes tangibles de un sistema informático) y de igual modo, un software (componentes lógicos de un sistema informático) Sin embargo, no basta una perspectiva netamente instrumental haciendo referencia a los elementos físicos que facilitan la visualización de los documentos digitales, existe además, un componente lógico señalando que este tipo de documentos “contienen un mensaje de texto alfanumérico, conformado por los bits, formado por ceros y unos que se procesan sobre un soporte, llámese cinta o disco (en general, soporte electrónico) que está en principio destinado a durar en el tiempo.”. Con base en lo anterior, se puede afirmar que este tipo de documentos poseen características que los diferencian de aquellos producidos en soporte papel, esencialmente, por el uso de símbolos que se registran en un soporte y en un medio al que las personas no pueden acceder de manera directa por lo cual es necesario descifrarlos.
A partir de estas perspectivas sobre el documento digital, parece poder deducirse de forma argumentativa que lo que distingue a este documento digital de un documento en soporte papel es que en su gestión interviene de forma directa la tecnología. El documento digital si bien es diferente en el soporte, comparte con el documento en papel una misma función.
Preservación digital
Como consecuencia de la producción masiva de documentos digitales, surge simultáneamente la necesidad crear estrategias que permitan asegurar su preservación a largo del tiempo. En otras palabras, las estrategias de preservación documental ya no se relacionan únicamente con el soporte papel y otros documentos tangibles sino que también debe contemplar el tratamiento de los documentos digitales. En este sentido “la preservación digital comprende acciones específicas cuyo fin ulterior y a largo plazo es asegurar la permanencia y acceso del contenido de documentos digitales a lo largo del tiempo y las tecnologías, independientemente de su soporte, formato o sistema”. Para llevar a cabo este propósito es necesario emprender actividades que contemplen tanto su mantenimiento y protección, como su resguardo de manera anticipada para prevenir futuros deterioros o daños en la información. Se busca principalmente que existan los medios para identificar, mantener y preservar para siempre la información registrada pues constituyen el registro del pasado, permite entender el mundo actual, y sienta las bases para la construcción permanente de conocimiento.
El contenido informativo de los documentos digitales es uno de los aspectos sobre los cuales están dirigidos los esfuerzos de la preservación digital, ya que la preservación supone llevar a cabo tareas como la conservación preocupándose no solo por el mantenimiento del objeto, sino también, y principalmente por su contenido informativo.
Por esta razón la preservación de los documentos digitales centra su desarrollo en mantener la capacidad de visualizar, recuperar y utilizar de forma adecuada la información, sin dejar de lado, las frecuentes transformaciones que sufre el entorno tecnológico. Incluso en un sentido tradicional, la preservación ha estado enfocada a la forma física de los documentos, sin embargo, aspectos como el desarrollo de la tecnología, la aparición del documento digital, el alcance y concepto que se conoce como preservación documental ha necesitado una evolución y adaptación que va más allá de la integridad física del objeto para intervenir en la integridad intelectual y el aseguramiento de la información con todos sus elementos asociados.
Se habla del mantenimiento a largo plazo de la cadena de bits y la accesibilidad continuada del contenido. De manera que es importante también determinar estrategias que faciliten no solo la preservación del soporte, es decir el hardware que permite la visualización de la información, sino que garanticen de igual modo, el contenido del documento, esto es, la información contenida, que puede trascender a las generaciones para ser consultada por cualquier persona independientemente del dispositivo que utilice para ello. La preservación entonces, busca soluciones que permitan la permanencia y accesibilidad a la infinita cantidad de información digital que se está produciendo hoy en día.
La preocupación surge al cuestionarse sobre si esta información digital llegará a las generaciones venideras, siendo más profundo el problema al evaluar la fragilidad de los soportes y el frecuente cambio en las tecnologías. Esta perspectiva es señalada donde la preservación digital se define como las actividades necesarias para asegurar el acceso continuado a materiales digitales hasta cuando sea necesario, a pesar de los obstáculos que representan los fallos en los soportes o los cambios tecnológicos. Los planteamientos anteriormente señalados coinciden en dos aspectos fundamentales que debe observar la preservación digital. El primero sobre aquellas acciones, procedimientos, directrices o procesos que posibiliten de forma ilimitada el acceso a la información independiente del soporte y el contenido. En otras palabras, la preservación digital no existiría si no se mantiene la posibilidad de acceder a los recursos digitales. El segundo aspecto hace referencia a la disponibilidad de estos documentos a lo largo del tiempo. Se habla entonces de preservación a largo plazo la cual garantiza que la información pueda ser consultada en los próximos años superando obstáculos como la obsolescencia de los soportes y la evolución de la tecnología. Finalmente, estas labores de preservación deben implementarse teniendo en cuenta elementos cambiantes como el deterioro de los medios físicos y tecnológicos a través de los cuales se gestionan los contenidos digitales.
Como conclusión se puede decir que la preservación digital hace referencia al conjunto de estrategias tendientes a conservar la información que se encuentra en formato digital bien sean estos documentos, fotografías, archivos de audio, bases de datos entre otros. Su objetivo es facilitar y perfeccionar acciones tan importantes como el: acceder, visualizar, descifrar, interpretar, comprender e interactuar con documentos u objetos digitales de forma valida y sencilla con el propósito de facilitar la transferencia de datos e información que aseguren la gestión de conocimiento en concordancia con la evolución de la humanidad. La preservación a largo plazo aplica a documentos electrónicos y digitales independientemente del formato, y requiere a su vez, de la elaboración de un plan de preservación a largo plazo que incluyen acciones para asegurar además su conservación, su acceso y disponibilidad a lo largo del tiempo. También es importante mencionar que el almacenamiento digital es fácil, sin embargo, la preservación no lo es. Preservar digitalmente la información almacenada, organizada, conlleva no solo una planeación estratégica como política institucional, requiere a su vez una serie de gastos emanados de las transformaciones y/o actualizaciones tecnológicas tanto del software como de los hardware presentes en la sociedad del conocimiento que evoluciona con rapidez.
Buenas prácticas para la preservación digital
En la sociedad actual las organizaciones están creando, recibiendo y gestionando continuamente documentos digitales, lo cual, ha suscitado nuevos retos para las administraciones teniendo en cuenta el alto valor que representan la información en medio digital no solo para la toma de decisiones, sino para la garantizar la conformación y preservación del patrimonio digital institucional. Se habla entonces de las buenas prácticas para la gestión de documentos digitales los cuales poseen características especiales que exigen acciones específicas para garantizar su preservación durante el tiempo que sea necesario. Desde una perspectiva legal el Archivo General de La Nación (2014), en su compilación normativa establece que “una norma de buenas prácticas es un documento que nos indica cómo actuar siguiendo metódicamente unas pautas establecidas, reconocidas y aceptadas por un colectivo profesional o social suficientemente representativo y aprobado.” (p. 8). En este concepto se identifican elementos que reafirman la complejidad de la preservación digital pues si se habla de buenas prácticas, previamente a la conformación y divulgación de las mismas, es necesario que un grupo interdisciplinar de profesionales al interior de las organizaciones establezcan y aprueben de forma conjunta los procedimientos que guiaran las labores de preservación digital institucional. En efecto, la preservación digital surge como respuesta a un problema de carácter tecnológico que no debe ser abordado desde esta perspectiva únicamente. Dentro de una organización la preservación digital incluye aspectos administrativos, financieros y legales los cuales, en conjunto, le dan forma a un programa de preservación que facilitará la consolidación del patrimonio documental institucional. Las buenas prácticas de preservación digital deben estar enmarcadas en una política institucional que cuente con un firme respaldo financiero, un apoyo a nivel gerencial y por supuesto, un compromiso administrativo por parte de los funcionarios que intervienen en la cadena de preservación. Por este motivo, la definición de las buenas prácticas debe contemplar la resolución de preguntas como ¿Que guardar y porqué guardarlo?, ¿Dónde guardarlo?, ¿Hasta cuándo guardarlo?, ¿Cómo encontrarlo después?, ¿Cómo hacer que se mantenga inalterado?, ¿Cómo evitar que se vuelva obsoleto?
No olvides que en caso de ser necesario, puedes contactarnos para mejorar el proceso de laboratorio y administrativo de tu organización a través software 100% confiable y seguro. Recuerda que en deappharma somos expertos en la materia, por lo que procesos complejos no representa un reto para nosotros, debido a que tenemos en mente los aspectos relevantes de cumplimiento.
¡Contáctanos! y conoce de que manera te vamos a ayudar.
¡Únete a nuestra comunidad en redes!
29, Jun 2021
Revisión de estado validado de método analíticos.
Uno de los varios procesos de control analítico dentro de la industria, es el seguimiento o mantenimiento del estado validado y/o estado de control de métodos analíticos. No es una tarea fácil!! ya que para realizar una correcta revisión, el entorno en el que gira el proceso de mantenimiento validado radica en el acceso a documentos y en la obtención de datos que se asocian directamente a la esencia del método, como son: primera validación y parámetros de adecuabilidad históricos.
Concepto:
El concepto de ciclo de vida, vincula el desarrollo de productos y procesos, por lo que se debe adquirir conocimiento para abordar la revisión.
Validación métodos y calidad de los medicamentos.
La validación efectiva del método contribuye significativamente a asegurar la calidad de los medicamentos. Lo básico, es comprender el principio de garantía de calidad. Este principio describe que se debe producir un medicamento que sea apto para el uso previsto.
Este principio incorpora el entendimiento de que existen las siguientes condiciones:
a) La calidad, la seguridad y la eficacia están diseñadas o integradas en el producto.
b) La calidad no puede garantizarse adecuadamente simplemente mediante el producto en proceso y terminado, inspección o prueba.
Un programa de validación exitoso depende de la información y el conocimiento del método, así como, de la comprensión del proceso de desarrollo analítico. Este conocimiento es la base para establecer un enfoque para el control del analítico, que da como resultado certidumbre en la calidad y atributos evaluados. Los científicos analíticos deben:
- Comprender las fuentes de variación (se puede evaluar durante la validación o con la revisión de los datos de validación).
- Detectar la presencia y el grado de variación (análisis de datos obtenidos en la validación y en el histórico de datos de liberación, sin embargo, esto no mide directamente el método).
- Controlar la variación de una manera acorde con el riesgo, que representa para el método que afecta los datos de liberación del producto.
Descripción del proceso analítico en tres etapas:
Etapa 1 – Diseño del proceso analítico: el proceso analítico se define durante este etapa, basada en el conocimiento adquirido a través de actividades de desarrollo.
Etapa 2 – Validación del proceso analítico: durante esta etapa, el diseño analítico se evalúa para determinar si método es capaz de producir resultados reproducibles.
Etapa 3 – Verificación continua del proceso analítico: la garantía continua se obtiene durante la rutina analítica, de tal manera, que se pueda verificar que el proceso permanece en un estado de control.
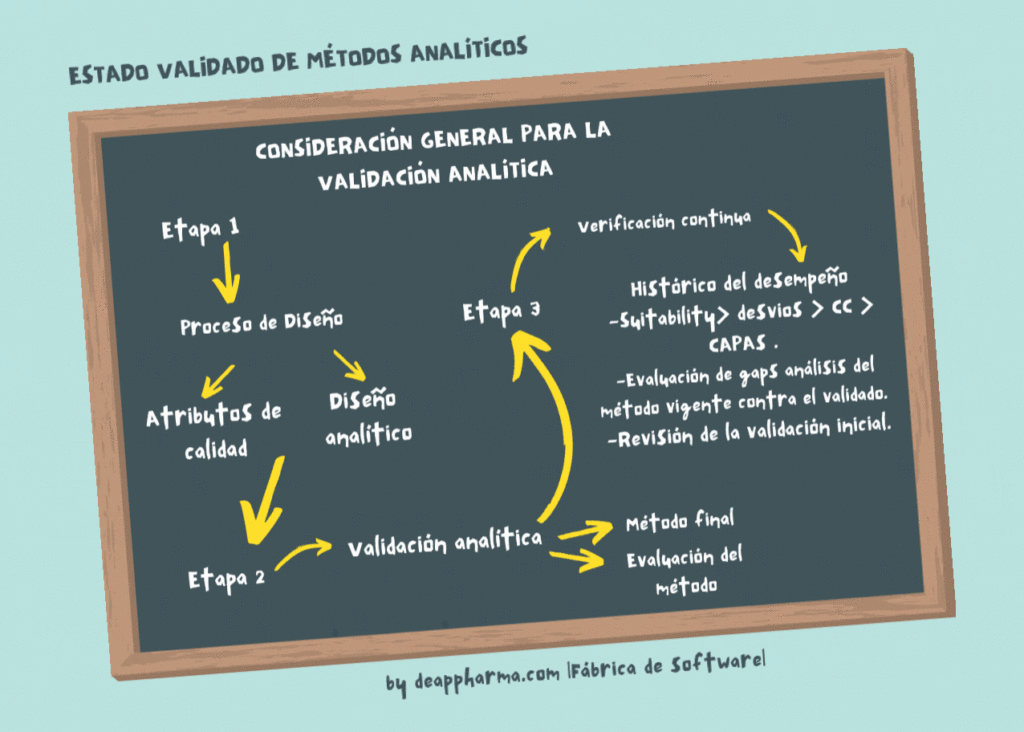
Los puntos relevantes de evaluación a la etapa 3, son:
- Requisitos de idoneidad históricos del sistema (platos teóricos, resolución, factor de coleo, factor de simetría, factor de capacidad y/o tiempos de retención de componentes).
- Parametrización y evaluación de las pruebas de desempeño acordes al método analítico.
- Revisión de los ajustes a las condiciones de operación indicadas en el procedimiento analítico vigente vs los descritos en la validación y/o transferencia inicial.
- Hallazgos o desviaciones, directamente relacionadas al desempeño del método analítico.
Si una evaluación basada en riesgos es utilizada como herramienta, se deben considerar otros factores. Los cuales pueden conducir a cambios en un procedimiento analítico y/o reemplazo con un nuevo método, se puede considerar los siguiente:
- Un ejercicio nuevo de transferencia;
- Una posible revalidación, sea parcial o total, o,un nuevo ejercicio de validación o,
- Un estudio de comparabilidad de métodos analíticos, es una opción factible.
En algunos casos, cambios en el fármaco o sustancias dentro del proceso de fabricación también deben ser evaluados como parte de la revisión de estado validado.
Recurso analítico «software».
Como se menciono anteriormente, la revisión de estado validado de un método analítico radica en que tan disponible y correcta fue la ejecución de este. Por lo que, la disposición de la información debe ser consistente. De otra manera será difícil concluir.
eADMxL el software de cumplimiento de deappharma.com , le ayudara con el control del proceso de estado validado mediante sus funciones especificas de «Revisión de estado validado» y «Monitoreo de vigencias».
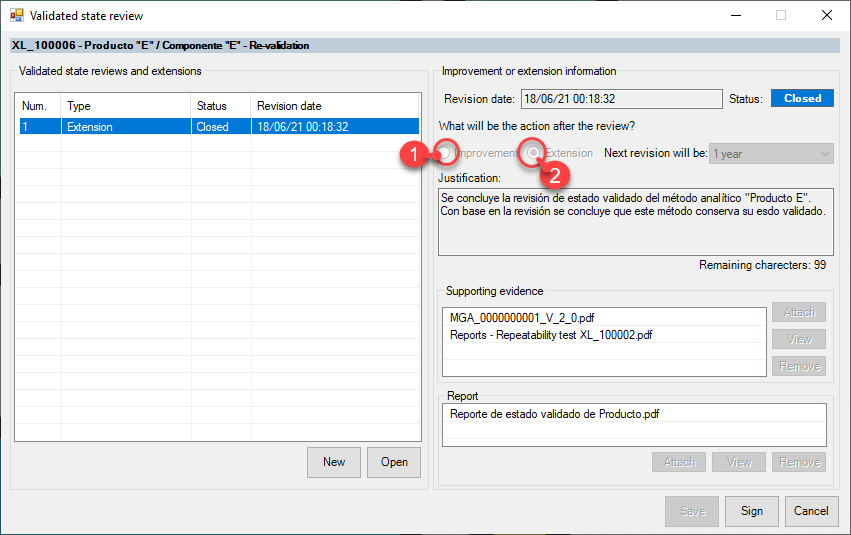
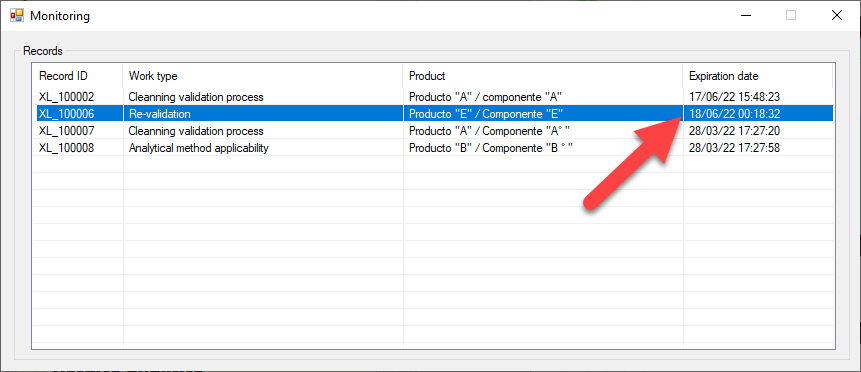
Algunas preguntas relevantes, que le ayudaran a definir el estado de control y/o mantenimiento, son:
- El método fue planteado y validado en concordancia con su categoría?
- La estadística paramétrica es integra?
- Los resultados de validación analítica son consistentes y claros?
- Si es un método compendial, los datos de pruebas de robustez tolerados están documentados?
- Los criterios de “Suitability” del sistema, se mantienen a través de los análisis?
- Las condiciones analíticas establecidas en el método final (preparación , condiciones de análisis, columna etc.) son las mismas que están descritas en el reporte de validación del método?
- Si hay cambios al método, se registran y se alinean a un control de cambio y se emite un CaPa al método y con esto evaluar el impacto a la validación?
- Qué tan recurrentes son las desviaciones o justificaciones asociadas al método analítico?
- Si la validación analítica sigue vigente, puedo hacer un revisión de estado validado antes de su fin expiración si surgen problemas?
No olvides que en caso de ser necesario, puedes contactarnos para mejorar el proceso de laboratorio y administrativo de tu organización a través software 100% confiable y seguro. Recuerda que en deappharma somos expertos en la materia, por lo que procesos complejos no representa un reto para nosotros, debido a que tenemos en mente los aspectos relevantes de cumplimiento.
Referencias.
- Analytical Procedures and Methods Validation for Drugs and Biologics Guidance for Industry
- Pharmaceutical quality system ICH Q10.
- Guidance for Industry Process Validation: General Principles and Practices.
¡Contáctanos! y conoce de que manera te vamos a ayudar.
¡Únete a nuestra comunidad en redes!
7, Jun 2021
La esencia del Límite de Cuantificación en métodos analíticos por HPLC.
Importancia de la validación.
Validación se puede definir como “encontrar o evaluar la verdad de algo”.
Cuando un método analítico es usado para generar resultados acerca de las características de la sustancia de interés (eg., fármaco o medicamento), es vital que los resultados sean confiables, ya que estos serán usados como base para la toma de decisiones en relación, con la definición de la forma de administración del fármaco o medicamento al paciente.
Un estudio de validación, el cual deriva en un método analítico tiene como finalidad el asegurar que los resultados obtenidos sean fidedignos (ALCOA), siempre que estos sean obtenidos dentro del proceso analítico.
¿Pero en donde o porque radica la importancia del proceso de validación?
La importancia radica en que cada día, se realizan en el mundo un alto número de análisis, relacionados al monitoreo de compuestos orgánicos, estas mediciones son utilizadas en algunas situaciones para la toma de decisiones, en áreas como son; control de calidad (liberación), manufactura (evaluación de procesos), áreas analíticas (estudios de estabilidad), proyectos de transferencia analítica.
El límite de Cuantificación “Concepto”
Límite de cuantificación, es la habilidad de un método para detectar y cuantificar la cantidad mínima de un analítico en una muestra, cual puede ser detectada con precisión y exactitud.
El límite de cuantificación es un parámetro de cuantificación de ensayo, para los niveles bajos de los compuestos en las matrices farmacéuticas, y es usada particularmente para la determinación de impurezas y/o productos de degradación.
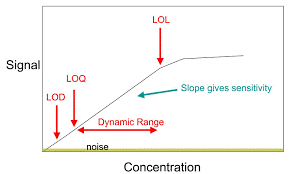
Planteamiento de la prueba.
Se preparan 6 muestras de placebo adicionadas con el componente principal Api (polvo) (Active Pharmaceutical Ingredient) es lo recomendable. Ya que de esta manera podrás retar la esencia de la preparación analítica. Es recurrente contar con una cantidad limitada de impureza, por lo que, se podrá plantear la prueba con un estándar ya disuelto, para posteriormente ser adicionado a las soluciones placebo (n=6) y de esta manera optimizar el uso.
En caso de no contar con el placebo o matriz farmacéutica se podrán preparar 6 muestras independientes de producto terminado caduco o producto que es sometido a pruebas de estrés controlada. La concentración analítica de la muestra estará determinada en relación al 50% ó 0.05% respecto a la concentración establecida, es decir, respecto al límite de sustancias relacionadas, productos de degradación conocidos y/o desconocidos establecidos en tu método de análisis. El restante porcentual será completado con producto terminado, en los que el cálculo de recobro se vera ajustado por la diferencia que habrá entre el nivel evaluado y el blanco (muestra enriquecida) para ajustar la señal de trabajo.
Estadística y parámetros a evaluar (primarios).
- Promedio individual
- Promedio de n=6
- Desviación estándar de n=6
- Mínimo de n=6
- Máximo de n=6
- Intervalos de confianza del valor de “µ”
- T critico
- T estadístico
- Intervalo de confianza de ““µ” %
- P-value
Criterios de aceptación.
La evaluación deberá mostrar las señales del pico de interés diferenciadas de la señal ruido:
- Señal ruido del pico de interés mínimo de 10.
- Los recobros de las 6 muestras deben cumplir con el recobro especificado.
- Debe mostrarse homocedasticidad en los resultados globales n=6, p-value mayor al 0.05
- Los intervalos de confianza deben incluir el valor del 100%.
- El coeficiente de valoración debe ser “<= “al establecido 5, 10, 15 ó 20 % según aplique el nivel % del límite evaluado.
Obtención de la concentración a evaluar.
Las principales formas de obtención del parámetro son:
1.-Basado en evaluación visual: la evaluación visual puede usarse para métodos no instrumentales, pero también puede usarse con métodos instrumentales. el límite de cuantificación se determina mediante el análisis de muestras con concentraciones de analito y estableciendo el nivel mínimo al cual el analito puede ser detectado de manera confiable.
2.-Basado en señal a ruido: este enfoque solo se puede aplicar a los procedimientos analíticos que muestran una línea de base ruido. La determinación de la relación señal / ruido se realiza comparando señales de muestras con bajas concentraciones conocidas de analito con las del blanco muestras y establecer la concentración mínima a la cual el analito puede ser detectado y cuantificado de manera confiable. Generalmente se considera una relación señal / ruido entre o 10: 1 aceptable para estimar el límite de cuantificación.
3.-Basado en la desviación estándar de la respuesta y la pendiente: el límite de cuantificación (QL) puede expresarse como:
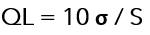
Donde:
σ = desviación estándar de la respuesta.
S = la pendiente de la curva de calibración.
La pendiente S puede estimarse a partir de la curva de calibración del analito.
-Basado en la curva de calibración: se debe estudiar una curva de calibración específica utilizando muestras que contengan un analito en el rango del Límite de Cuantificación. La desviación estándar residual de una línea de regresión o el estándar la desviación de las intersecciones con el eje y de las líneas de regresión pueden usarse como la desviación estándar.
Recomendaciones.
-El límite de cuantificación y el método utilizado para determinar el límite de cuantificación debe ser presentado, el límite debe validarse posteriormente mediante el análisis de un número adecuado de muestras conocidas o preparadas a la concentración del límite de cuantificación.
-La evaluación del parámetro de Limite de Cuantificación siempre se lleva a cabo con enfoque cuantitativo, es decir, tratar el ensayo como si fuese una valoración.
-El recobro no solo se puede ver afectado por la matriz también se ve alterado por la posible adhesión a componentes del contenedor / cierre, por ejemplo, vial de vidrio, válvula dosificadora. En general, un procedimiento de preparación de muestra más simple dará como resultado una menor variación de la recuperación.
No olvides que en caso de ser necesario, puedes contactarnos para mejorar el proceso de laboratorio y administrativo de tu organización a través software 100% confiable y seguro. Recuerda que en deappharma somos expertos en la materia, por lo que procesos complejos no representa un reto para nosotros, debido a que tenemos en mente los aspectos relevantes de cumplimiento.
Proceso de linealidad del sistema y LOQ controlado y gestionado con eADMxL.
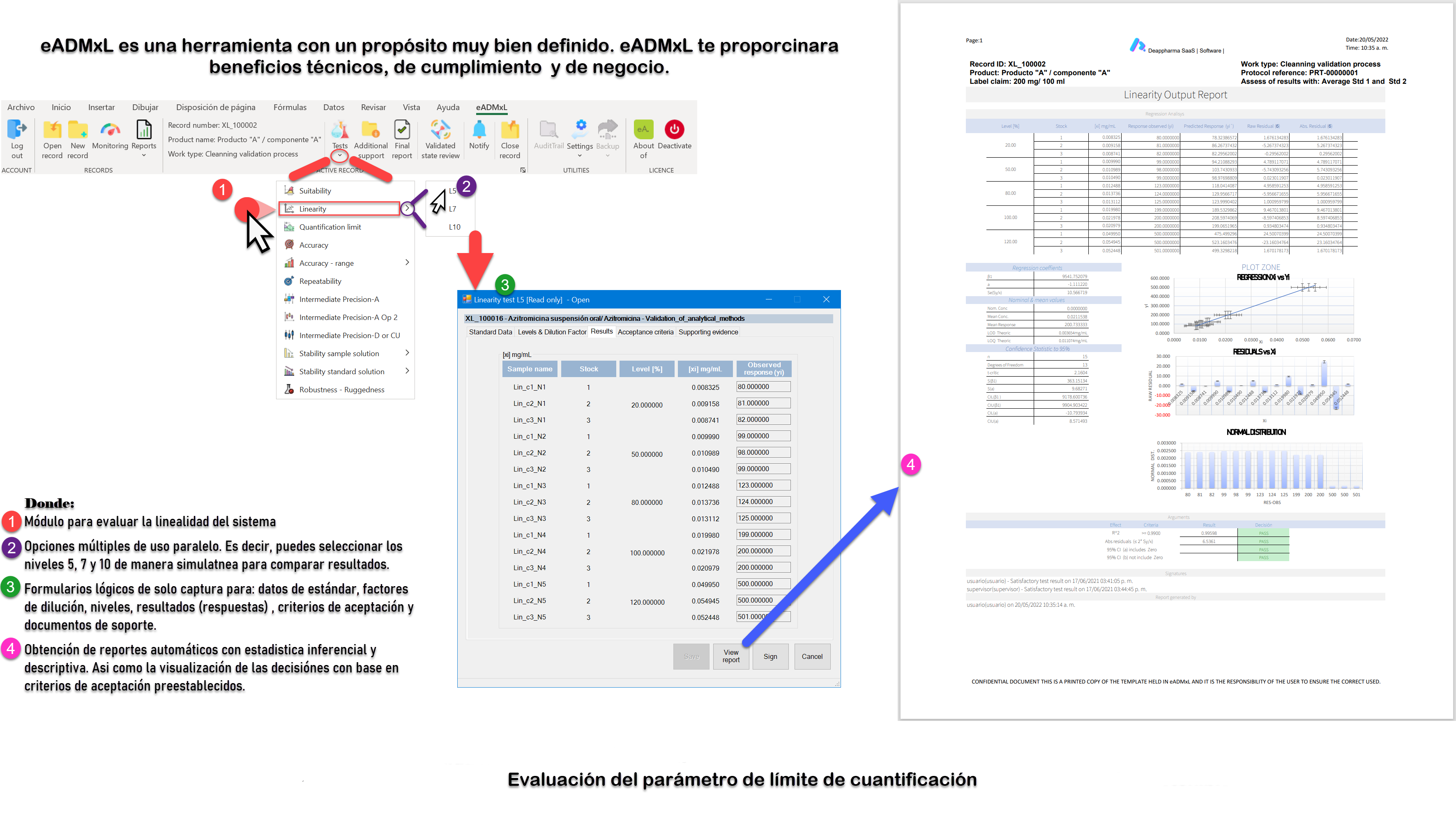
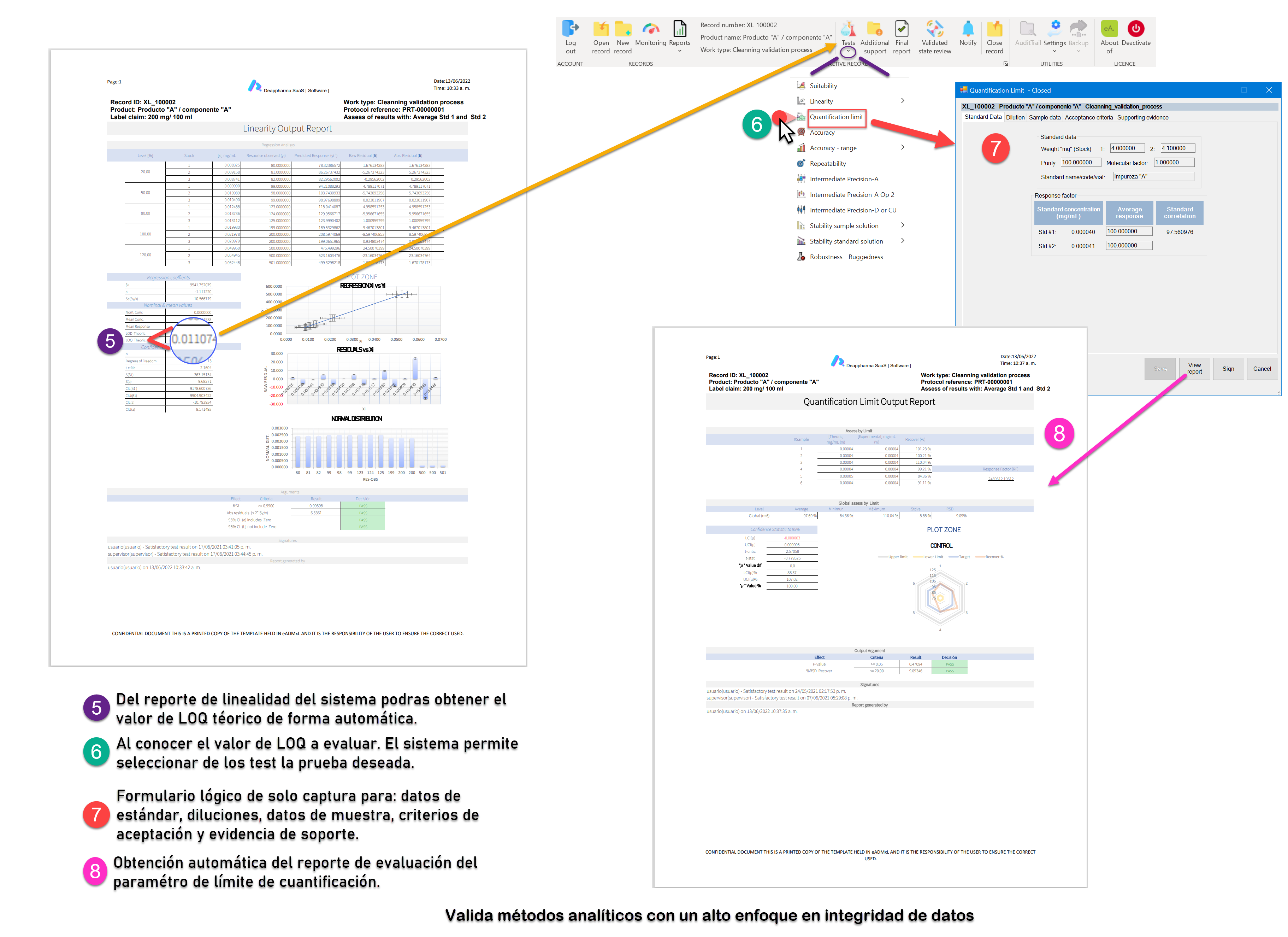
No olvides que, en caso de ser necesario, puedes contactarnos para mejorar el proceso de laboratorio y administrativo de tu organización a través software 100% confiable y seguro. Recuerda que en deappharma contamos con un software que te ayudara a controlar tu proceso de validación de métodos analíticos. Somos expertos en la materia, por lo que procesos complejos no representa un reto para nosotros, debido a que tenemos en mente los aspectos relevantes de cumplimiento.
Referencias.
- NORMA OFICIAL MEXICANA NOM-059-SSA1-2015, Buenas prácticas de fabricación de medicamentos.
- FDA analytical procedures and methods validation for drugs and biologics
- WHO guidelines on validation – appendix 4 analytical method validation
- ICH Harmonised tripartite guideline validation of analytical procedures: text and methodology q2(r1).
¡Contáctanos! y conoce de que manera te vamos a ayudar.
¡Únete a nuestra comunidad en redes!